Гидрат - окись - бериллий
Cтраница 1
Гидрат окиси бериллия амфотерен. Нормальные соли бериллия, так же как и бериллаты, в водном растворе сильно гидролизированы, так как и основные и кислотные-свойства у гидрата окиси бериллия выражены слабо. [1]
Гидрат окиси бериллия амфотерен. [2]
Гидрат окиси бериллия почти нерастворим в воде; он не является щелочью, но при действии кислот образует соли. [3]
Так как гидрат окиси бериллия ( глюцин) осаждается, начиная с растворимой соли окиси бериллия, то следует высушить полученный после фильтрации осадок. Во время опытов каждый осадок фильтрации помещали на фарфоровую капсюлю, следя за тем, чтобы толщина слоя составляла 3 см; сушку вели в сушилке с инфракрасными лампами Мазда 250 вт, расположенными в шахматном порядке на расстоянии 20 см над высушиваемым продуктом. [4]
Получается из гидрата окиси бериллия. [5]
Ordt) 1 гидрат окиси бериллия, выделившийся при кипячении раствора бериллата щелочного металла, значительно плотнее, чем гидрат, свежеосажденный аммиаком, и отличается от него своей нерастворимостью в углекислом калии и трудной растворимостью в углекислом аммонии; он та же значительно труднее растворяется в разбавленных кислотах. Если к раствору прибавить большой избыток едкой щелочи, то при кипячении гидрат окиси бериллия не выделяется. [6]
Карбонат бария осаждает гидрат окиси бериллия. [7]
Ordt) J гидрат окиси бериллия, выделившийся при кипячении раствора бериллата щелочного металла, эначи-гельво плотнее, чем гидрат, свежеосажденный аммиаком, и отличается от riero своей нерастворимостью в углекислом калии и трудной растворимостью в углекислом аммонии; он та же значительно труднее растворяется з разбавленных кислотах. Если к раствору прибавить большой избыток едкой щелочи, то при кипячении гидрат окиси бериллия не выделяется. [8]
Карбонат бария осаждает гидрат окиси бериллия. [9]
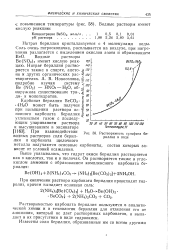 |
Растворимость сульфата бериллия в воде. [10] |
Выше указывалось, что гидрат окиси бериллия растворяется как в кислотах, так и в щелочах. [11]
Так, гидрат окиси лития LiOH - щелочь, гидрат окиси бериллия Ве ( ОН) 2 характеризуется амфотерными свойствами. Гидрат окиси бора Н3ВО3 и гидрат двуокиси углерода Н2СО3 представляют собой слабые кислоты. Гидрат окиси натрия NaOH, как и LiOH, - щелочь. [12]
При действии аммиака на растворы солей бериллия выпадает осадок гидрата окиси бериллия, обладающий амфотерными свойствами. Гидроокись бериллия растворяется в щелочах, углекислом аммонии с образованием бериллатов, а также в кислотах с образованием хорошо растворимых солей. [13]
Основные соединения, имеющие практическое значение: окись бериллия ( ВеО) - белый мелкодисперсный легкий порп-шок; гидрат окиси бериллия - Be ( ОН) а - мелкодисперсный аморфный порошок белого цвета; сернокислый бериллий ( BeSOj 4Н2О) - белый порошок; хлорид бериллия ( Ве2С1г); фтористый бериллий ( BeF2) - белое кристаллическое вещество. При нагревании дает фторокись бериллия. [14]
Гидрат окиси бериллия не является щелочью. В соединениях бериллий двухвалентен. [15]
Страницы: 1 2