Гидрат - окись - бериллий
Cтраница 2
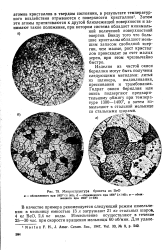 |
Микроструктура брикета из ВеО. [16] |
Изделия из чистой окиси бериллия могут быть получены следующими методами: литья из шликера, выдавливания, прессования и трамбования. Гидрат окиси бериллия или окись подвергают предварительному обжигу при температуре 1300 - 1400, а затем измельчают в стальной мельнице со стальными шарами. [17]
Бериллий - двухвалентный металл, менее активен по сравнению с литием; с водой не взаимодействует и ее не разлагает. Гидрат окиси бериллия Ве ( ОН) 2 практически нерастворим в воде. [18]
Образующийся при этом растворимый фторид бериллия выщелачивают горячей водой и в кислый раствор добавляют едкий натр до нейтрализации. Образующийся NaF возвращают обратно в процесс, а гидрат окиси бериллия прокаливают до окиси. [19]
Способ щелочной переработки заключается в спекании руды с известью во вращающейся печи с последующей грануляцией и разложением серной кислотой. Раствор сульфата бериллия обрабатывают аммиаком, при этом выпадает гидрат окиси бериллия. [20]
Ordt) 1 гидрат окиси бериллия, выделившийся при кипячении раствора бериллата щелочного металла, значительно плотнее, чем гидрат, свежеосажденный аммиаком, и отличается от него своей нерастворимостью в углекислом калии и трудной растворимостью в углекислом аммонии; он та же значительно труднее растворяется в разбавленных кислотах. Если к раствору прибавить большой избыток едкой щелочи, то при кипячении гидрат окиси бериллия не выделяется. [21]
Ordt) J гидрат окиси бериллия, выделившийся при кипячении раствора бериллата щелочного металла, эначи-гельво плотнее, чем гидрат, свежеосажденный аммиаком, и отличается от riero своей нерастворимостью в углекислом калии и трудной растворимостью в углекислом аммонии; он та же значительно труднее растворяется з разбавленных кислотах. Если к раствору прибавить большой избыток едкой щелочи, то при кипячении гидрат окиси бериллия не выделяется. [22]
По характеру защиты черных металлов, меди и ее сплавов серебряное покрытие является катодным. Для защиты от потускнения серебряные покрытия подвергают одному из видов дополнительной обработки: пассивированию, оксидированию, палладированию, родированию, покрытию гидратом окиси бериллия. [23]
Гидрат окиси бериллия амфотерен. Нормальные соли бериллия, так же как и бериллаты, в водном растворе сильно гидролизированы, так как и основные и кислотные-свойства у гидрата окиси бериллия выражены слабо. [24]
При действии воды на магний эта реакция протекает очень медленно. Бериллий устойчив по отношению к воде. Это объясняется тем, что гидраты окисей бериллия и магния труднорастворимы и предохраняют металлы от дальнейшего действия воды. Однако при нагревании магний реагирует с водой более энергично. Скорость реакций с водой увеличивается от магния к барию. В этом же порядке растет растворимость их гидратов окисей и понижается устойчивость металлов к действию воздуха. [25]
Имеется указание на синтез ди-н-пропилбериллия в работе Каура [ 49а ], который, нагревая металлический бериллий с дипропилртутью в запаянной трубке при 130 - 150 С, наблюдал быстрое исчезновение металла и появление металлической ртути. С; на воздухе интенсивно дымит, но не воспламеняется; при охлаждении до - 17 С принимает вид густой маслянистой жидкости, но не затвердевает. Водой бурно разлагается с большим выделением газа и с образованием на стенках сосуда осадка гидрата окиси бериллия. [26]
Ядовитость соединений бериллия вызывает необходимость исследовать воздух на содержание в нем бериллия. Критической концентрацией считается 0 01 мкг / м5, следовательно, определению подлежат еще меньшие количества бериллия. В таких случаях хорошие результаты дает спектральный метод: воздух просасывается через бумажный фильтр, который затем сжигают и обрабатывают соответствующим образом для получения осадка гидрата окиси бериллия на носителе - гидрате окиси алюминия. [27]
Бериллий получают электролизом его расплавленных солей. Благодаря небольшому удельному весу, его применяют для изготовления легких сплавов. Бериллий устойчив к коррозии на воздухе благодаря образующейся на его поверхности защитной пленке окиси. Окись бериллия ВеО - белое, очень тугоплавкое вещество. Гидрат окиси бериллия имеет ясно выраженный амфотерный характер, чем резко отличается от гидроокисей других элементов той же подгруппы и напоминает алюминий. Бериллий, как и алюминий, растворяется в щелочах. [28]
Страницы: 1 2