Гидрат - окись - титан
Cтраница 1
Гидрат окиси титана Ti ( OH) 4 амфотерен; основные его свойства преобладают. Как и у олова, существуют две формы гидрата двуокиси титана: а-форма, легко растворимая в кислотах, и реформа, нерастворимая в разбавленных кислотах. Соли титановой кислоты ( титанаты) в растворах полностью гндролизованы. [1]
Рентгеноанализ гидратов окиси титана показывает, что орто-кислота является аморфным соединением, мета-кислота обладает слабо выраженной кристаллической структурой, которая полностью совпадает с кристаллической структурой двуокиси титана модификации анатаз. [2]
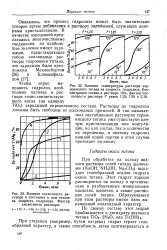
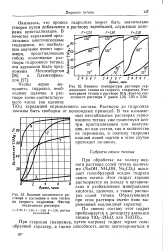
Как видно из представленного уравнения, образование гидрата окиси титана, выпадающего в осадок, идет постепенно. Образующиеся промежуточные продукты длительное время находятся в коллоидном состоянии. Проведенные нами количественные наблюдения показали, что через сутки в растворе остается 79 - 90 % от исходного уровня титана. К 6 - м суткам содержание титана достигает 0 18 - 0 20 мг / л независимо от начальной его концентрации и в последующие дни не изменяется. Такое постоянство концентраций указывает на то, JTO выпадение титана в осадок в результате гидролиза происходит до уровня, соответствующего пределу растворимости образующегося гидрата. [3]
 |
Рабочая секция. [4] |
При отмывке полимеризата от продуктов разложения каталитического комплекса образуются гидрат окиси титана и хлорокись алюминия. [5]
Для этих реакций пользуются раствором сернокислого титана или раствором гидрата окиси титана в соляной кислоте. [6]
Как указывалось выше, в силу гидролиза тетрахло-рида выпадает желеобразный осадок гидрата окиси титана. Находящийся в коллоидном состоянии гидрат окиси титана придает воде молочную окраску, резко снижает прозрачность воды. Так при концентрации титана 200 мг / л прозрачность исходной воды падает до 2 5 - 4 см и только спустя 10 суток начинает постепенно восстанавливаться. [7]
Для проведения гидролиза в раствор сернокислого титана добавляют отдельно приготовленные зародыши в форме коллоидного раствора гидрата окиси титана. [8]
При обработке на холоду водного раствора солей титана щелочами ( NaOH, NH4OH, Na2CO3) выпадает гелеобразный осадок гидрата окиси титана. Этот гидрат хорошо растворяется на холоду в органических и разбавленных минеральных кислотах, щелочах, а также растворах солей титана. Образующиеся при этом растворы имеют явно выраженный коллоидный характер. [10]
При обработке на холоду водного раствора солей титана щелочами ( NaOH, NH4OH, Na2CO3) выпадает гелеобразный осадок гидрата окиси титана. Этот гидрат хорошо растворяется на холоду в органических и разбавленных минеральных кислотах, щелочах, а также растворах солей титана. Образующиеся при этом растворы имеют явно выраженный коллоидный характер. [12]
В мерную колбу емкостью 250 мл отбирают 10 мл электролита, добавляют 0 2 г FeCl3 ( для лучшей коагуляции гидрата окиси титана), разбавляют водой до 50 мл, приливают 50 мл 20 % раствора NaOH, перемешивают и осторожно нагревают до кипения. Затем колбу охлаждают до комнатной температуры, доливают раствор водой до метки, перемешивают и фильтруют через сухой фильтр в сухую колбу. [13]
Одним из основных свойств растворов сернокислого титана является их способность к гидролизу при разбавлении или при нагревании с выделением в осадок гидрата окиси титана. [14]
Гидраты полуторных окислов [ Fe ( OH) 3, A1 ( OH) 3, Сг ( ОН) 3 и гидрат окиси титана Ti ( OH) 4 ] осаждают 10 % - ным раствором аммиака. Титан, алюминий и железо могут-быть определены без предварительного отделения других металлов ( см. стр. [15]
Страницы: 1 2