Гидрат - соль
Cтраница 1
Гидраты солей отличаются от гидратов газов и жидкостей. Последние имеют кубические строения молекул и плавятся инконгруэнтно; структура гидратов солей не кубическая, и они плавятся конгруэнтно. [1]
Гидрат соли с меньшим количеством атомов натрия содержит четыре молекулы кристаллизационной воды. [2]
Ряд гидратов солей можно перевести в безводное состояние осторожным нагреванием в вакууме в присутствии подходящего осушающего средства, причем в этом случае не наблюдается заметного гидролитического разложения. Это справедливо для таких солей, как ВаС12 или Со12, если не предъявляется особых требований к их чистоте. [3]
 |
Давление пара гидратов соли при постоян. [4] |
При образовании гидратов солей кривые давления пара усложняются, причем давление зависит не только от температуры, но и от числа молекул кристаллизационной воды. [5]
Характерные свойства гидратов солей кислородных кислот, оксидов и гидроксидов объясняются способностью образовывать гид-роксильные связи, обусловленные электростатическим притяжением частично экранированных атомов водорода. [6]
Диэлектрическая постоянная: гидраты солей, 100 - 400 К, 500 - 20 000 гц. [7]
Точка состава этого гидрата соли А на вторичной проекции совпадает с вершиной А. По достижении точки М выпавший гидрат обезвоживается. Затем по мере испарения начинает выпадать в осадок соль А. В эвтонической точке Э ч дополнительно будет выпадать и двойная соль ВС до полного усыхания раствора. [8]
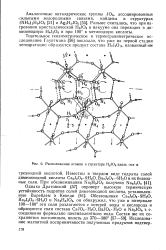 |
Расположение атомов в структуре HjJOj вдоль оси а. [9] |
Известны в твердом виде гидраты солей димезоиодной кислоты Ca2J2O9 9Н2О, Ba2J2Og 6Н2О и их безводные соли. [10]
Однако следует рассмотреть ЭПР гидратов солей меди ( П), которые обладают почти октаэдрической симметрией. При температуре выше примерно 50 К наблюдается изотропный спектр ЭПР. В области температур 10 - 50 К изотропный спектр исчезает и появляется новый - анизотропный. Характер анизотропного спектра указывает на тетрагональное искажение кристаллического поля. При наличии искажения, обусловленного эффектом Яна - Теллера, поверхность потенциальной энергии имеет три неглубоких минимума для искажений вдоль главных осей кристалла. При очень низких температурах ион находится в состоянии, соответствующем одному из этих минимумов, и обладает анизотропным спектром ЭПР. При высоких температурах заселены более высокие колебательные состояния и ион быстро переходит из одного состояния в другое, в результате чего наблюдается изотропный спектр ЭПР. [11]
При дальнейшем испарении раствора выделяется гидрат соли В. Для любого состава системы ( например, т3) состав жидкой фазы расположен в точке т пересечения кривой растворимости с лучом кристаллизации, проведенным из вершины кристаллизации гидрата К. [12]
 |
Слой, образованный из соединенных вершинами групп. [13] |
В этом простейшем из типов гидратов солей все молекулы воды связаны с катионами. Количество атомов кислорода, которое может быть размещено вокруг иона металла, определяется отношением радиусов гм: Го, и так как связи М - О, в сущности, являются электростатическими по своей при-имеют координационные полиэдры, кото-ионных кристаллов. [14]
 |
Группировки протон - вода в гидратах. [15] |
Страницы: 1 2 3 4 5