Шестиводной гидрат
Cтраница 1
Аналогичные шестиводные гидраты образуют многие жидкие галоидо-замещенные углеводороды, например хлороформ. Они обладают гораздо более низкой упругостью диссоциации, чем гидраты газов. [1]
Кристаллы шестиводного гидрата хлористого магния тщательно перемешать с хлористым аммонием ( двукратное количество по весу), поместить в тигель и прокалить на пламени газовой горелки. [2]
Какие же вещества образуют молекулярные шестиводные гидраты. В настоящее время известно несколько десятков этих соединений. Гидраты получены почти для всех наиболее часто встречающихся в лабораторной практике газов. Были получены гидраты и для трех благородных газов. Гидрат аргона получил еще в 1896 г. Вийяр [31], компримируя аргон до 150 атм. [3]
При растворении 1 граммолекулы безводного хлорида кальция с образованием шестиводного гидрата выделяется 17 41 ккал. Тепловой эффект растворения шестиводной соли равен - 4 31 ккал. [4]
Почти для всех обычных в лабораторной практике газов были открыты шестиводные гидраты. Исключение составляют лишь О2, N2, PL, CO, a также два инертных газа: Не и Ne. Для того чтобы грубо оценить упругость диссоциации гипотетического гидрата неона, сопоставим атомные характеристики инертных газов и упругости диссоциации их. [5]
На основании тензиометрических измерений необходимо отметить, что вещества, образующие шестиводные гидраты, не образуют никаких других гидратов ни с большим, ни с меньшим числом молекул воды. [6]
В виде иллюстрации влияния растворимости исследуемого вещества в водной и органической фазах на коэффициент распределения можно привести данные Кейзера, Ципрса и Кер-мана [7.] по растворимости шестиводного гидрата нитрата уранила в воде и различных растворителях, а также и соответствующие коэффициенты распределения. [7]
Расход хлористого кальция на высушивание определяется влагосодержанием высушиваемой жидкости. В процессе сушки хлористый кальций может поглощать количество воды, соответствующее образованию шестиводного гидрата его ( около 100 % от его веса), однако на практике чаще всего ориентируются на поглощение хлористым кальцием 30 - 50 % влаги, считая на вес загруженного в аппарат хлористого кальция. Этот аппарат представляет собой стальной цилиндрический котел, имеющий внутри сетчатую обтянутую полотном трубу /, которая располагается концентрически цилиндру котла. По окончании загрузки в аппарат пускается сжатый воздух ( труба 2), который заставляет циркулировать высушиваемую жидкость через сетчатую трубу, заполненную хлористым кальцием. [8]
Подробный критический анализ литературного материала позволяет сделать вывод, что молекулярные шестиводные кристаллогидраты образуют вещества, которые ограниченно растворимы в воде и практически не диссоциированы на ионы в водном растворе. Действительно, спирты, которые смешиваются с водой во всех отношениях, не дают шестиводных гидратов. Галоидоводороды, которые полностью или в значительной мере диссоциированы на ионы в водном растворе, дают низшие гидраты, кристаллическая решетка которых, невидимому, построена из ионов, а не из молекул ( см. гл. Для аммиака, который в водном растворе образует ионы аммония, шестиводный гидрат тоже не известен. [9]
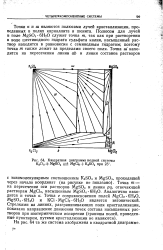 |
Квадратная диаграмма водной системы. [10] |
Точки к и ш являются полюсами лучей кристаллизации, проведенных в полях карналлита и шенита. Полюсом для лучей в поле MgSO4 6Н2О служит точка т, так как при растворении в воде шестиводного гидрат а сульфата калия, насыщенный раствор находится в равновесии с семиводным гидратом; поэтому точка т также лежит за пределами своего поля. [11]
Далее от этой точки идет третья ветвь кристаллизации следующего гидрата хлорида стронция. Химический анализ показал, что в соли содержится 36.21 % хлор-иона или 80.97 % хлористого стронция, что близко отвечает шестиводному гидрату. Полученная изотерма растворимости исследуемой системы аналогична диаграмме, установленной предыдущими исследователями. [12]
В предпоследнем столбце приведены упругости диссоциации при 0 С некоторых известных гидратов и оценка их для гипотетических гидратов. В последнем столбце указаны упругости газов при 0 С над водным расвором, содержащим на 1 мол. Это сопоставление показывает, что упругость диссоциации шестиводных гидратов НВг и НС1 должна быть более 720 мм, а упругость этих газов над водным раствором, содержащим на 1 мол. Следовательно, эти гидраты получить вообще невозможно. [13]
Визуальным наблюдением за изменением внешнего вида кристаллов семиводного гидрата в процессе нагревания установлено, что при 45 С появляется некоторое количество жидкости. Образующуюся при этом твердую фазу удается выделить путем обработки CoS04 7Н20, нагретым до 60 С этиловым спиртом. Потеря веса при нагревании этой фазы до 350 С говорит о том, что соль отвечает составу шестиводного гидрата. [14]
Настоящее исследование имело целью изучить теплоемкость растворов, в которых перемена окрашивания свидетельствует о существовании в растворе различных соединений с водой. Замечательным примером в этом отношении служит водный раствор хлористого кобальта. При обыкновенной температуре и ниже насыщенный раствор розового цвета, около 40 цвет становится фиолетовым, а выше - синим. Кроме шестиводного гидрата розового цвета, существуют еще два кристаллических гидрата. На изменение состава водного раствора под влиянием температуры указывают явления, открытые при исследовании растворимости СоС122 и упругости пара раствора в зависимости от температуры. Растворимость СоС12 в зависимости от температуры выражается двумя прямыми линиями, соединенными кривой. Точки перелома отвечают температурам, при которых замечается изменение цвета раствора. В полном соответствии с кривой растворимости находится кривая, изображающая изменение упругости пара в зависимости от температуры. Как в первом случае, так и здесь изменение цвета сопровождается переломом в течении кривой. [15]
Страницы: 1 2