Низший гидрат
Cтраница 3
Сравнивая водородные соединения Si с углеводородами, должно ждать, что первые продукты замещения водорода гидроксилом будут носить спиртовый характер, а только высшие - кислотный. Это обстоятельство чрезвычайно важно для понимания природы низших гидратов, которые известны для кремния. Если мы представим, что из первых гидратов будет отниматься вода ( так, муравьиная кислота есть СН ( ОН) 3 без воды), то получим различные низшие гидраты, отвечающие кремневодороду. Такие неполные гидраты кремния, или, правильнее сказать, кремневодорода, получены первый раз Велером ( 1863), изучались Рейтером ( 1865) ( доп. [31]
Обычно для определения давления диссоциации применяется статический метод в условиях постоянной температуры. Этот метод отнимает много времени и требует довольно сложной аппаратуры, причем особое затруднение представляет его использование при высоких температурах. Между тем, знание зависимости давления диссоциации от температуры, а также теплот дегидратации имеет большое практическое значение для выяснения условий получения окислов, безводных солей или их низших гидратов. Эти данные нужны и для многих технологических расчетов. Поэтому метод быстрого определения давления диссоциации, хотя и не такой точный, как статический, может приобрести большое значение и найти широкое применение. [32]
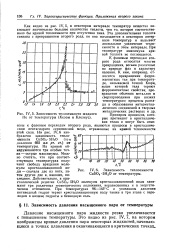 |
Зависимость теплоемкости жидкого Примером процессов кото. [33] |
На кривой обнаруживаются три особые точки - острые максимумы. Можно считать, что при соответствующих температурах получают свободу вращения молекулы кристаллизационной воды - сначала две из пяти, затем другие две и, наконец, последняя. Действительно, в кристаллической решетке CuSOi 5Н2О молекулы кристаллизационной воды занимают три различных геометрических положения, неравноценных и в энергетическом отношении. При температурах 96 - 145 С и указанном давлении пятиводный гидрат теряет кристаллизационную воду также в три этапа с переходом в низшие гидраты и безводную соль. [34]
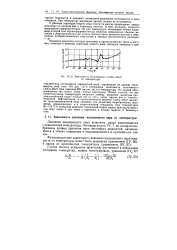 |
Зависимость теплоемкости от температуры. [35] |
На рис. IV, 6 изображена зависимость теплоемкости CuSO4 - 5HzO ( при давлении 692 мм рт. ст.) от температуры. На кривой обнаруживаются три особые точки-острые максимумы. Можно считать, что при соответствующих температурах получают свободу вращения молекулы кристаллизационной воды-сначала две из пяти, затем другие дае и, наконец, последняя. Действительно, в кристаллической решетке CuSO j - 5HsO молекулы кристаллизационной воды занимают три различных геометрических положения, неравноценных и в энергетическом отношении. При температурах 96 - 145 С и указанном давлении пятиводный гидрат теряет кристаллизационную воду также в три этапа с переходом в низшие гидраты и безводную соль. [36]
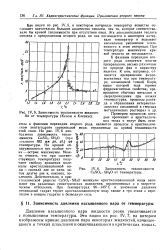 |
Зависимость теплоемкости жидкого Be от температуры ( Кезом и Клезиус. [37] |
К фазовым переходам второго рода относятся многие превращения, весьма различные по природе фаз и характеру явления. К ним, например, относятся превращения ферромагнитных тел при температуре, называемой точкой Кюри, выше которой тела теряют ферромагнитные свойства, превращение обычных металлов в сверхпроводники при низких температурах, процессы распада и образования интерметаллических соединений в твердых металлических растворах и др. Примером процессов, которые протекают в кристалличе-ких телах и могут быть отнесены к фазовым переходам второго рода, являются процессы в кристаллическом пентагидрате сернокислой меди, отраженные на кривой теплоемкости этой соли. На рис. IV, 6 изображена зависимость тепло - SO емкости CuSO4 5Н2О ( при лгшленни 692 мм рт. ст.) от температуры. На кривой обнаруживаются три особые точки - острые максимумы. Можно считать, что при соответствующих температурах получают свободу вращения молекулы кристаллизационной воды - сначала две из пяти, затем другие две и, наконец, последняя. Действительно, в кристаллической решетке CuSQi-S O молекулы кристаллизационной воды занимают три различных геометрических положения, неравноценных и в энергетическом отношении. При температурах 96 - 145 С и указанном давлении пятиводный гидрат теряет кристаллизационную воду также в три этапа с переходом в низшие гидраты и безводную соль. [38]
Важный шаг к выяснению строения этих соединений был сделан Пау-лингом в 1929 году. Он предположил, что центральный октаэдр AsO j очружен шестью тетраэдрами W04 и имеет с ними общие вершины. Для этих иэнов существует другая структура, состоящая из колец шести октаэдров WOd, каждый из которых имеет два общих ре эра с другими октаэдрами. Однако может быть, что общими являются тольк) вершины полиэдров, состоящих из вольфрама и кислорода, а не ре фа. Это определенно наблюдается у 12-кислот, для ионов которых Пауллнг предложил трехмерную структуру. В этой структуре центральный тетраэдр Р04 окружен полиэдрической оболочкой состава W ] 2O ] 8, в которой каждый атом W соединен с тремя другими атомами кислорода. Хотя эта структура была очень бтизка к действительной структуре, которую мы опишем ниже, она, конечно, не могла представлять структуру иона в безводной кислоте или в низших гидратах, так как содержит 36 атомов водорода. [39]
Страницы: 1 2 3