Гидрид
Cтраница 1
Гидриды вносятся в реакционную смесь растворенными, и только КаВЩ и некоторые другие можно прибавлять порциями в твердом виде. В случае алюмогидрида лития используют его небольшой избыток ( 5 - 10 %), учитывая, что часть соединения реагирует со следами воды и других гидроксилсодержащих примесей. После завершения восстановления непрореагировавший гидрид и образовавшийся комплекс гидролизуют, для чего осторожно прибавляют воду или водные растворы хлорида натрия, хлорида аммония или гидроксида натрия. Если реакционная смесь содержит большой избыток L1A1H4, то для разложения реакционной смеси рекомендуется использовать этилацетат, который медленно реагирует с гидридом, давая этиловый спирт. Последний не мешает дальнейшему выделению продуктов реакции. [1]
Гидрид реагирует с алкинами в углеводородных растворителях путем час-присоединения с образованием тронс-винилаланов ( 1) из алкинов-1 и цис-винилаланов кз цизамещеиных алкинов. [2]
Гидрид [97, 312] представляет собой темно-серый пирофорный порошок, обладающий большой химической активностью. Гидрид урана растворяется в НМОз, в концентрированной НС1О4 и горячей концентрированной FhSCU. Разлагается при нагревании 400 в вакууме. [3]
Гидриды MH8 V образуют неметаллы двух коротких периодов ( бор образует гидриды особого типа, см, гл. [4]
Гидриды являются очень активными веществами, энергично взаимодействующими с НгО, СЬ, галогенами. [5]
Гидриды - специфические материалы, широко применяемые в современной промышленности. [6]
Гидриды широко применяются в порошковой металлургии. [7]
Гидриды с ионным типом связи энергично реагируют с водой и влагой воздуха, давая в растворе сильную щелочную реакцию. В мелкораздробленном состоянии при действии влаги все гидриды воспламеняются. Некоторые гидриды, такие как гидрид церия, воспламеняются во влажном воздухе даже в виде кусочков. Еще энергичнее они взаимодействуют с водными растворами кислот и большинством химических растворителей. С солями, имеющими аналогичные свойства, эти гидриды образуют системы с простой эвтектикой, с остальными солями, большинством газов, с органическими веществами, реагируют как очень сильные восстановители. Из-за большой реакционной способности ионных гидридов необходимо очень тщательно подходить к подбору материалов аппаратуры при их получении и исследовании. [8]
Гидрид анализируют на содержание водорода разложением навески гидрида раствором хромной кислоты и измерением выделяющегося количества водорода. Магний определяют осаждением фосфатами. [9]
Гидрид не содержит примеси магния и может быть использован без дальнейшей очистки. [10]
Гидриды гафния, аналогично гидридам титана и циркония, получают в виде порошков в установке типа установки Снвертса ( см. стр. Для получения более высоких по содержанию водорода составов проводят гидрирование при более низких температурах. [11]
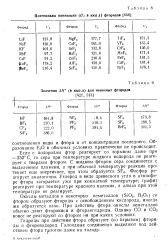 |
Значения АН ( в ккал для неионных фторидов. [12] |
Гидриды при действии фтора образуют ( со взрывом) фториды и фтороводород. Галоидные соединения выделяют под действием фтора галоген даже на холоду. [13]
Гидриды являются очень активными веществами, энергично взаимодействующими с НгО, СЬ, галогенами. [14]
Гидриды щелочных и щелочноземельных моталлон быстро разрушаются под денстипсм влаги и кислорода воздуха, что ипогда сопровождается самовозгоранием. Поэтому хранить их следует в заиаянных ампулах, в атмосфере сухого водорода пли инертного газа. [15]
Страницы: 1 2 3 4