Гидрид
Cтраница 2
Гидрид - Н3 лития получают реакцией обмена. [16]
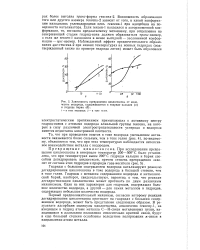 |
Зависимость превращения циклогексена от количества водорода, содержащегося в гидриде кальция ( а и гидриде бария ( б. [17] |
Гидриды с большим содержанием водорода катализируют реакцию дегидрирования циклогексена в токе водорода в большей степени, чем в токе гелия. Гидриды с меньшим содержанием водорода и металлический барий, наоборот, свидетельствуют, вероятно, о том, что реакция дегидрогенизации циклогексена может протекать по двум различным механизмам. Один из них характерен для гидридов, содержащих большое количество водорода, а другой - для самих металлов и гидридов, содержащих небольшое количество водорода. [18]
Гидрид карбонила кобальта - белое кристаллическое вещество, которое плавится при температуре 26 С. Выше этой температуры он довольно быстро разлагается и чрезвычайно токсичен. [19]
Гидрид в кипящем водном ( 2 %) изопропаноле, содержащем следы соляной кислоты, катализирует перенос водорода от изопропилового спирта к разнообразным субстратам. При восстановлении дифенилацетилена был получен промежуточный комплекс X, гидролизующийся с образованием 1 ( ыс-стильбена. [20]
Гидриды и амиды щелочных металлов МеН и MeNHa представляют собой бесцветные кристаллические вещества солеобразного характера, в которых водород и группа NH2 играют роль анионов. [21]
Гидриды ( МеНа) - бесцветные кристаллические солеобразные вещества, в которых водород играет роль аниона. В соответствии с этим они взаимодействуют с водой и спиртами с выделением водорода. [22]
Гидрид известен только для палладия. [23]
 |
Изменение структуры полуторных окислов Р. м. в зависимости от темп-ры и порядкового номера элемента. А - гексагональная, В - тригональная ( ромбич. или моноклинная, С - кубическая.. [24] |
Гидриды имеют гранецентрированную кубич. [25]
 |
Изменение структуры полуторных окислов Р. м. в зависимости от темп-ры и порядкового номера элемента. А - гексагональная, В - тригональная ( ромбич. или моноклинная, С - кубическая.. [26] |
Гидриды обладают различной термохи-мич. Гидрид церия при комнатной темп-ре реагирует с азотом, а при нагревании до 800 - 900 переходит в нитрид. На воздухе гидрид воспламеняется с образованием смеси окисла и нитрида. Для предотвращения подобного разрушения гидрида применяется его обработка осушенным углекислым газом. Рг и Nd при комнатной темп-ре инертны к водороду и только при 300 - 400 активно его абсорбируют. [27]
Гидриды - соединения с водородом - применяются в электровакуумной технике, металлургии, металлокерамическом синтезе как замедлители и отражатели в ядерной технике, как источники чистейшего водорода в исследовательских работах. [28]
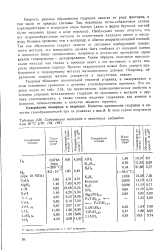 |
Содержание водорода в некоторых гидридах при 20 С ( 197, 194, 195. [29] |
Гидриды обладают значительной теплотой сгорания, и выдерживают в этом отношении сравнение с лучшими углеводородными горючими. Это хорошо видно из табл. 2.54, где представлены термодинамические свойства и теплоты сгорания металлических гидридов по сравнению с метаном и другими углеводородами, а также такими жидкими гидридами, как аммиак и гидразин, используемыми в качестве жидкого горючего. [30]
Страницы: 1 2 3 4