Гидрид - железо
Cтраница 1
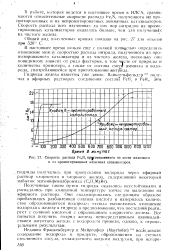 |
Скорость распада Fe4N, приготовленного из чисто железного и из промотированных железных катализаторов. [1] |
Гидриды железа известны уже давно. [2]
Наименее устойчивый гидрид железа C5H5Fe ( CO) 2H превращается в димер уже при комнатной температуре, а также при действии кислорода воздуха. Гидриды Сг и Мо разлагаются при 57 С, а гидрид W - при 180 С. [3]
Осаждение гидрида железа из смеси растворов CeHsMgBr - f - FeCl3 [2] начинается при исходном соотношении компонентов 3: 1, о чем свидетельствует начало поглощения водорода, и при увеличении этого соотношения до 6: 1 и особенно до 12: 1 выход продукта повышался и увеличивалась скорость реакции. [4]
Мйкровключения ( окислы и гидриды железа, марганца и их силикаты), а при отливке в сырые формы - макровключения. [6]
За последнее время синтезированы некоторые производные гидрида железа, содержащие гидридный водород наряду с органическими аддендами. [7]
Метод получения из органических растворов подробно описан для гидридов железа ( см. стр. [8]
В процессе образования и разложения твердого раствора водорода или неустойчивых гидридов железа изменяются параметры кристаллической решетки железа и возникают значительные напряжения внутри металла. [9]
Маловероятно, чтобы присоединение водорода к катиону протекало через образование индивидуальных соединений гидрида железа л - СрРе ( СО) 2Н и СН3СН СН2 с последующим повторным присоединением гидрида к олефину, поскольку в процессе восстановления не удалось осуществить передачу железа к гексену-1 или бутадиену. [10]
Согласно второй гипотезе, так называемой водородной, выделяющийся во время реакции водород вследствие появления в его структуре гидрида железа сообщает стали водородную хрупкость. [11]
Согласно второй, так называемой водородной, гипотезе выделяющийся при реакции водород придает стали водородную хрупкость вследствие появления в его структуре гидрида железа. Считается вероятным, что выделяющийся водород вступает в реакцию с находящимися по границам зерен загрязнениями с образованием газообразных продуктов реакции; последние, обладая слабой способностью диффундировать через металл, способствуют развитию повышенных напряжений и образованию вследствие этого трещин. [12]
Поскольку метод получения не дает точно установленных продуктов в отношении их состава, структуры, устойчивости и воспроизводимости метода, последний описан в общем виде для гидридов железа ( см. стр. [13]
Эти и подобные им исследования для других гидридов впервые иавели на мысль, что водород во всех соединениях связан не с железом, а с магнием, образуя либо смешанный гидрид железа и магния, либо комплексное соединение, в состав которых, кроме указанных компонентов, входит органический растворитель. Изучение ИК-спектров показало, что в так называемом гидриде железа, осажденном реактивом Гриньяра, иет полос связи Fe - Н, но зато обнаруживаетси линия, характерная для гидрида магния. [14]
Мне представляется, что своеобразная форма кривой перенапряжения водорода на железо связана с влиянием различных примесей. Влияние этих примесей в том, что они способствуют образованию на поверхности железного катода пленки гидридов железа. [15]
Страницы: 1 2