Гидрид - лантан
Cтраница 2
Было также подтверждено, что для этих фаз константы решетки могут варьировать и уменьшаются при повышении содержания водорода. На основании электронографического исследования гидрида лантана [96] установлено, что образцы состава LaH2 имеют структуру типа CaF2, причем атомы водорода занимают все тетраэдрические междуузельные позиции. [16]
Редкоземельные металлы взаимодействуют с водородом медленно при комнатной температуре, быстрее при более высокой температуре ( 250 - 300), иттрий-при 400 в вакууме. Образуются красно-коричневый гидрид церия, черный гидрид лантана, блестящие, аморфные, индиго-синие гидриды неодима и празеодима, хрупкий сине-серый гидрид иттрия YHj. [17]
Поэтому между ними и солеобразными гидридами принципиально возможно наличие постепенного перехода. Хорошим примером соединения такого переходного типа является гидрид лантана. Металлический лантан уже на холоду поглощает водород с довольно большим выделением тепла ( около 20 ккал / г-экв), причем образующийся продукт по составу приблизительно отвечает формуле LaHs - Оба эти обстоятельства сближают La со щелочноземельными металлами. Однако, в отличие от их водородных соединений, гидрид лантана представляет собой не бесцветные кристаллы, а черный порошок, причем содержание в нем водорода зависит от давления и начинает уменьшаться уже при слабом нагревании. Оба эти обстоятельства указывают скорее на то, что поглощенный водород находится не в химически связанном, а в растворенном состоянии. Тем самым намечается переход от рассматриваемых производных к группе металлообразных гидридов. [18]
 |
Растворимость водорода в палладии. [19] |
Поэтому между ними и солеобразными гидридами принципиально возможно наличие постоянного перехода. Хорошим примером соединения такого переходного типа является гидрид лантана. [20]
Рентгенографическое исследование структуры гидридов редкоземельных элементов, проведенное Росси [127] в 1934 г., показало, что гидриды лантана, церия и празеодима имеют кубическую гранецен-трированную решетку, причем постоянные решетки увеличены по сравнению с кубической решеткой металла. Кроме того, Росси установил, что если образцы гидридов лантана и цезия откачивать вакууме, то содержание водорода, уменьшается, а постоянные решетки несколько увеличиваются. [21]
Рентгенографическое исследование структуры гидридов редкоземельных элементов, проведенное Росси [127] в 1934 г., показало, что гидриды лантана, церия и празеодима имеют кубическую гранецен-трированную решетку, причем постоянные решетки увеличены по сравнению с кубической решеткой металла. Кроме того, Росси установил, что если образцы гидридов лантана и цезия откачивать в вакууме, то содержание водорода уменьшается, а постоянные решетки несколько увеличиваются. [22]
Поданным последних работ [160], состав продукта насыщения лантана водородом при комнатной температуре соответствует формуле ЬаНз. О приготовлении LaD3 сообщается в работе Виалларда [160]; свойства дейтерида близки к свойствам гидрида лантана. [23]
Поэтому между ними и солеобразными гидридами принципиально возможно наличие постепенного перехода. Хорошим примером соединения такого переходного типа является гидрид лантана. Металлический лантан уже на холоду поглощает водород с довольно большим выделением тепла ( около 20 ккал / г-экв), причем образующийся продукт по составу приблизительно отвечает формуле LaHs - Оба эти обстоятельства сближают La со щелочноземельными металлами. Однако, в отличие от их водородных соединений, гидрид лантана представляет собой не бесцветные кристаллы, а черный порошок, причем содержание в нем водорода зависит от давления и начинает уменьшаться уже при слабом нагревании. Оба эти обстоятельства указывают скорее на то, что поглощенный водород находится не в химически связанном, а в растворенном состоянии. Тем самым намечается переход от рассматриваемых производных к группе металлообразных гидридов. [24]
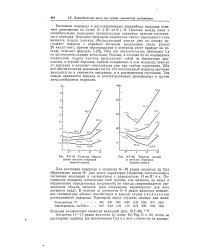 |
Теплоты образования летучих гидридов ( ккал / г-связь. [25] |
Поэтому между ними и солеобразными гидридами принципиально возможно наличие постепенного перехода. Хорошим примером соединения такого переходного типа является гидрид лангана. Металлический лантан уже на холоду поглощает водород с довольно большим выделением тепла ( около 20 ккал / г-экв), причем образующийся в конечном счете продукт по составу отвечает формуле LaHs. Оба эти обстоятельства сближают La со щелочноземельными металлами. Однако, в отличие от их водородных соединений, гидрид лантана представляет собой не бесцветные кристаллы, а черный порошок, причем содержание в нем водорода зависит от давления и начинает уменьшаться уже при слабом нагревании. Оба эти обстоятельства указывают на то, что поглощенный водород частично находится не в химически связанном, а в растворенном состоянии. Тем самым намечается переход от рассматриваемых производных к группе металлообразных гидридов. [26]
В случае элементов побочных подгрупп периодической системы ( если они склонны к образованию соединений с водородом) получаются главным образом металлообразные гидриды. Они часто не имеют стехиометрического состава. Иногда водород образует с металлами лишь твердые растворы, входя в кристаллическую решетку без изменения структуры. В некоторых слу-чаях, прежде всего для элементов побочных подгрупп IV и V групп, происходит структурное превращение, если количества поглощенного водорода превышают определенный предел. Подобные водородные соединения называются металлообразными гидридами. Промежуточное положение между металлообразными и солеобразными гидридами занимают гидриды побочной подгруппы III группы, и особенно гидрид лантана. [27]
В случае элементов побочных подгрупп периодической системы ( если они склонны к образованию соединений с водородом) получаются главным образом металлообразные еидриды. Они часто не имеют стехиометрического состава. Иногда водород образует с металлами лишь твердые растворы, входя в кристаллическую решетку бе изменения структуры. В некоторых случаях, прежде всего для элементов побочных подгрупп IV и Vгрупп, происходит структурное превращение, если количества поглощенного водорода превышают определенный предел. Подобные водородные соединения называются металлообразными гидридами. Промежуточное положение между металлообразными и солеобразными гидридами занимают гидриды побочной подгруппы III группы, и особенно гидрид лантана. [28]
В случае элементов побочных подгрупп периодической системы ( если они склонны к образованию соединений с водородом) получаются главным образом металлообразные гидриды. Они часто не имеют стехиометрического состава. Иногда водород образует с металлами лишь твердые растворы, входя в кристаллическую решетку без изменения структуры. В некоторых случаях, прежде всего-для элементов побочных подгрупп IV и V групп, происходит структурное превращение, если количества поглощенного водорода превышают определенный предел. Подобные водородные соединения называются металлообразными гидридами. Промежуточное положение между металлообразными и солеобразными гидридами занимают гидриды побочной подгруппы III группы, и особенно гидрид лантана. [29]
Страницы: 1 2