Гидрид - металл - группа
Cтраница 1
Гидриды металлов IV группы внешне и по основным технологическим свойствам очень похожи друг иа друга и поэтому технология получения их, особенно в виде порошков, практически ие отличается друг от друга. Только при получении компактных образцов имеются существенные различия потому, что должна учитываться более тонкая специфика металла. Методы синтеза компактных гидридов циркония разработаны гораздо лучше, чем для гидридов титана, и доведены до производства в заводском масштабе. [1]
Поэтому принципиальное значение приобретает способность гидридов металлов IVb группы образовывать двойные алюмо - и борогидриды солеоб-разного характера и низкой летучести и в некоторых случаях с высокой температурой плавления ( стр. В пределах подгруппы титана наблюдается повышение устойчивости и соле-образного характера двойных гидридов с ростом заряда ядра атомов. [2]
В работах [2-4] показано, что гидриды металлов IVB-VB групп являются активными катализаторами превращения углеводородов. [3]
Еще Хюттиг [18], а затем и Некрасов ( 10 ] считали, что гидриды металлов IV-Vb групп и редкоземельных металлов образуют как бы переход от металлических гидридов к соле-образным. [4]
Несколько странное впечатление складывается при анализе патентной литературы, посвященной использованию в качестве сокатализаторов гидридов металлов I-III групп. [5]
 |
Изотерма адсорбции. [6] |
В этой главе будут изложены более современные данные о структуре и основных физических свойствах гидридов металлов III-VIII групп периодической системы. [7]
Гидриды элементов подгруппы меди, как и подгруппы цинка, представляют по своим свойствам промежуточные соединения между типичными гидридами переходных металлов, подобными гидридам металлов V-VIII групп, и ковалент-ными гидридами элементов IV-Vila групп больших периодов периодической системы. [8]
Из газообразователей, в состав которых входят неорганические вещества, в патентной литературе упоминаются смеси металлов, способных образовывать амфотерные окислы, и едких щелочей, а также карбиды или гидриды металлов II группы, требующие для газообразования увлажнения композиции. [9]
 |
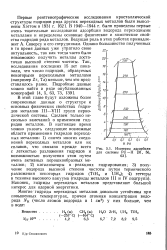
Давление ( /, развиваемое при термическом раз. [10] |
Из числа ХГО, в состав которых входят неорганические вещества, в патентной литературе упоминаются также смеси металлов, способных образовывать амфотерные окислы, и едких щелочей, а также карбиды или гидриды металлов II группы, требующие для газообразования увлажнения композиции. [11]
 |
Зависимость между электроотрицательностью металлов и типом связи в их гидридах. [12] |
Для гидридов металлов III группы характерно, что из трех атомов водорода, которые они максимально могут присоединять, первые два атома заполняют тетраэдрические пустоты и более прочно связаны, чем третий атом водорода, который находится в октаэдрическом положении, в большей мере отвечающем ионной связи. [13]
Гидриды переходных металлов более инертны по отношению к воде и водным растворам кислот. Только гидриды редкоземельных металлов гидролизуются водой, остальные гидриды к воде н водяным парам относительно устойчивы. С кислотами гидриды металлов IV-VIII групп реагируют в очень жестких условиях - при большой концентрации кислоты и нагревании. Плавиковая кислота разлагает все гидриды. [14]
 |
Энергия активации процесса самодиффузии водорода в гидридах переходных металлов. [15] |
Страницы: 1 2