Гидрид - щелочной металл
Cтраница 1
Гидриды щелочных металлов могут служить для получения водорода ( 1 кг гидрида лития при реакции с водой выделяет 2800 л водорода, а 1 кг гидрида натрия - 993 л), однако, ввиду большой реакционной способности и неудобства работы с ними, для этих целей предпочитают пользоваться гидридом кальция. [1]
Гидриды щелочных металлов мало токсичны, поскольку они не летучи, но попадая на кожу и особенно на слизистую оболочку ( глаза, верхние дыхательные пути), они вызывают сильное раздражение, обусловленное действием образующейся при гидролизе щелочи. Во всех случаях, когда работа с гидридами производится не в вытяжном шкафу, необходимо избегать пыления и пользоваться респиратором для защиты органов дыхания, а также перчатками. При попадании гидрида на кожу его следует стряхнуть или сдуть, и затем промыть пораженное место водой с мылом. [2]
Гидриды щелочных металлов используются как энергичные восстановители при получении ряда металлов. [3]
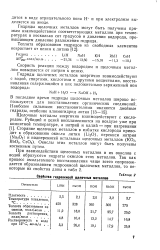 |
Свойства гидроокисей щелочных металлов. [4] |
Гидриды щелочных металлов могут быть получены прямым взаимодействием соответствующих металлов при температурах в несколько сот градусов и давлении водорода, превышающем давление разложения гидрида. [5]
Гидриды щелочных металлов имеют ионное строение. Металл входит в их состав в виде катиона, а водород - в виде аниона. [6]
Гидриды щелочных металлов растворяются в аммиаке. [7]
Гидриды щелочных металлов имеют ионное строение. Металл входит в их состав в виде катиона, а водород - в виде аниона. [8]
Гидриды щелочных металлов относятся к солеобраз-ным соединениям с ионным типом связи, реакционноспособны, используются как сильные восстановители. [9]
Гидриды щелочных металлов МеН - твердые соле-образные вещества ионного типа. [10]
Гидриды щелочных металлов имеют структуру типа Nad, однако положение атомов Н установлено только для LiH ( рентгеновская дифракция) и NaH ( дифракция нейтронов); расстояние Li - Н составляет 2 04 A, Na - Н - 2 44 А. Структура типа рутила для MgH2 была исследована нейтронографически на образце MgD2; расстояние Mg - Н составляет 1 95 А, кратчайшее расстояние Н - Н 2 49 А. [11]
Гидриды щелочных металлов являются очень сильными восстановителями. Окисление их кислородом воздуха в сухом состоянии идет сравнительно медленно, но в присутствии влаги процесс настолько ускоряется, что может привести к самовоспламенению гидрида. Особенно это относится к гидридам К, Rb и Cs. При взаимодействии NaH или КН с двуокисью углерода образуется соответствующая соль муравьиной кислоты. [12]
Гидриды щелочных металлов ( NaH - CsH) подвергаются термической диссоциации в пределах температур 400 - 450, гидрид же лития для этого требует более высокой температуры. [13]
Гидриды щелочных металлов в технике не применяются вследствие трудности их получения в значительных количествах: они используются для научно-исследовательских и препаративных целей. [14]
 |
Установка для получения гидрида лития из эфирных растворов. [15] |
Страницы: 1 2 3