Гидрид - палладий
Cтраница 2
Может быть, можно было бы получить лучший результат, если употреблять очень большие количества гидрида палладия. [16]
Причем внедрившиеся в решетку палладия атомы водорода, по-видимому, диффундируют, поскольку при пропускании через гидрид палладия электрического тока водород перемещается к катоду. Конечно, при внедрении кристаллическая решетка акцептора деформируется, иногда существенно. [17]
Некоторые факты позволяют предположить, что образуется беспорядочная нестехиометрическая фаза идеального состава PdH, но точная природа гидрида палладия все еще остается неопределенной. [18]
 |
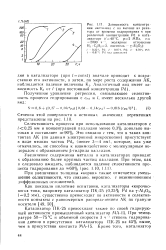
Кривые заряжения Pt / Pt-электрода в 0 5 М H2SO4 при различных температурах. [19] |
В исследуемом интервале температур, который ограничен температурами замерзания и кипения раствора электролита, зависимость логарифма давления диссоциации гидрида палладия от обратной температуры, как правило, получается линейной. [20]
 |
Структура и области существования гидридов хрома, никеля и палладия. [21] |
Такие же особенности обнаружены и в системе никель-водород, однако препараты гидрида никеля гораздо менее устойчивы, чем препараты гидрида палладия. [22]
Итак, первое различие - при образовании гидрида лития плотность по сравнению с металлом возрастает, а при образовании гидрида палладия - уменьшается. [23]
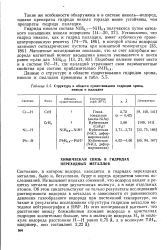 |
Структура и области существования гидридов хрома, никеля и палладия. [24] |
Такие же особенности обнаружены и в системе никель-водород, однако препараты гидрида никеля гораздо менее устойчивы, чем препараты гидрида палладия. [25]
Однако в рамках этих гипотез трудно объяснить наблюдаемую селективность палладиевых катализаторов, так как мало вероятно, что реакционная способность гидридов палладия по отношению к диеновым или ацетиленовым и олефиновым углеводородам различна. Более того, исследования последних лет [44] показали, что частицы металлического палладия размерами - 3 нм при обработке их водородом ( при давлении и, температуре, характерных для процесса гидрирования) ( i-гид-ридной фазы не образуют. С другой стороны, катализаторы, в которых размеры частиц палладия 10 нм, образуют ( - гидридную фазу, причем, селективность их в гидрировании существенно ниже, чем для высокодисперсных контактов. [26]
Вероятно, электронная пара смещена сильнее к атому металла в гидридах тех металлов, которые менее склонны отдавать электроны, например в гидридах палладия или никеля. А вот в гидридах скандия и урана, по-видимому, электронная пара сильно смещена в сторону водорода. Пожалуй, именно поэтому гидриды лантаноидов и актиноидов во многом похожи на гидриды щелочноземельных металлов. Действительно, ионные гидриды, например СаНо, это, в сущности, предельный случай смещения электронной пары к атому водорода. [27]
Это связано с тем, что в таких контактах АК ( по данным электронной микроскопии) присутствует в виде мелких частиц Pd, ( менее 3 - 4 нм), которые, как уже отмечалось, не способны к взаимодействию с молекулярным водородом с образованием - гидрида палладия. [29]
Известны лишь три интересных исключения, где наблюдается непрерывный переход от металла к фазе внедрения. Гидрид палладия, имея структуру типа NaCl, представляет в действительности предельно насыщенный твердый раствор и не обладает свойствами ковалентно-ионных карбидов, нитридов и окислов переходных металлов. В нем доминируют металлические связи, возникающие вследствие частичной коллективизации и перекрытия внешних / - электронов Р - оболочек палладия. Эти связи усиливаются благодаря участию в металлических связах коллективизированных s - электронов, внедряющихся в решетку атомов водорода. [30]
Страницы: 1 2 3 4