Гидрид - палладий
Cтраница 3
Если гипотеза Брюля относительно четырехвалентное кислорода правильна, то вода может присоединять к себе водород. Мне казалось, что гидрид палладия является подходящим восстановителем для осуществления этого присоединения. [31]
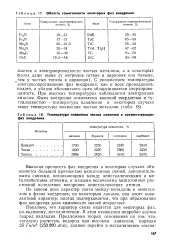 |
Область гомогенности некоторых фаз внедрения.| Температура плавления чистых металлов и соответствующих фаз внедрения. [32] |
Показано, что характер связи является для некоторых фаз, по-видимому, металлическим. В этом отношении подробно изучен гидрид палладия. [33]
Однако природа химической связи в гидридах переходных металлов и в настоящее время не вполне ясна. Первые теоретические работы были выполнены с гидридом палладия, физические свойства которого вплоть до недавнего времени были изучены лучше, чем свойства гидридов других металлов. Поэтому этот гидрид в течение многих лет служил моделью для всей группы рассматриваемых соединений. [34]
Хочется привести еще один факт, показывающий, как сложен вопрос о природе связи в гидридах внедрения и как трудно иногда найти безупречно поа-вильное объяснение экспериментальным данным. Если при низкой температуре осторожно удалить из гидрида палладия водород, то удается сохранить расширенную решетку, которая была у насыщенного водородом палладия. [35]
Природа тугоплавких соединений переходных металлов не столь ясна, как природа ионных или ковалентных кристаллов. Согласно одной гипотезе, предложенной Убеллоде [140] для гидрида палладия и распространенной затем на тугоплавкие карбиды, нитриды и другие соединения [141, 142], - часть валентных электронов с s - и р-уровней атома неметалла может переходить на незаполненный J-уровень атома переходного металла. С этой точки зрения донором оказывается неметалл, а акцептором - металлический атом. Палладий и водород имеют близкие электроотрицательности ( 2 0 и 2 13 эв) и сравнительно близкие потенциалы ионизации ( 8 33 и 13 59 эв), поэтому передача электрона от такого элемента, как водород, проявляющего в ряде случаев свойства катиона, к атому палладия - металла VIII группы со слабыми электроположительными свойствами представляется до известной степени возможной. Однако другие металлы VIII группы, по-видимому, не образуют гидридов со структурой типа NaCl. Металлы VII и VI групп, имеющие относительно высокие потенциалы ионизации и сравнительно большие значения электроотри-цательностей, гидридов такого типа также не образуют. [36]
Для того чтобы восстановление углекислоты протекало нормально, оно должно происходить в отсутствии как минеральных кислот, так и оснований. Я осуществил эти условия, применяя в качестве источника водорода in statu nascendi гидрид палладия. Действительно, при действии гидрида палладия на насыщенный раствор углекислоты в течение 30 дней я получил формальдегид, который мне удалось обнаружить в виде ангид-роформальдегиданилина и бромистого производного гексаметилентет-рамина. [37]
При более высокой температуре ( ЮО С) реакция становится нестереоспецифич-ной и при реакции ( 7) - фенилпропена образуются значительные количества продукта изомеризации. Такое исчезновение специфичности процесса может быть следствием реакций элиминирования - присоединения алкеновых комплексов гидридов палладия ( схема 606, ср. [38]
Поэтому для анализа экспериментальных данных, полученных с рутениевым, родиевым и платиновым катализаторами, можно было воспользоваться уравнениями ( 3); и ( 5), допуская, что механизм реакции на всех трех катализаторах одинаков. Поскольку палладиевый катализатор оказался весьма мало активным и можно предположить ( как это будет рассмотрено подробнее ниже), что во время каталитической реакции происходит образование гидрида палладия, значения k для этого катализатора рассчитаны не были. Постоянство полученных значений может служить подтверждением правильности предложенного механизма реакции. [39]
Хотя полученные таким образом результаты оказались положительными, но количество образовавшейся перекиси настолько мало, что опыты нельзя считать убедительными. Тем не менее я приведу здесь две серии опытов, не в качестве доказательства предложенной мною гипотезы, а как количественные данные, относящиеся к медленному окислению водорода in stalu nascendi из гидрида палладия. [40]
Исследование изомеризации октена-1 [76] в уксусной кислоте при использовании в качестве катализатора хлорида палладия показало, что изомеризация H - C5HiiCD2CH CH2 дает меньше дейтерия в концевых метальных группах образующихся октенов, чем можно было бы объяснить с помощью 1 3-переноса по я-аллиль-ному механизму. Эти результаты были объяснены, исходя из внутримолекулярного 1 2-переноса водорода, по которому при изомеризации н - С5НцСО2СН СН2 D переходит от С3 к С2, а Н переходит от С2 к d - Альтернативное объяснение, представленное в работе [77], основано на механизме присоединения - элиминирования гидрида палладия в сочетании со значительным изотопным эффектом при разрыве связей углерод-водород и предпочтительным анти-марковниковском присоединением гидрида. Высокое отношение выхода продуктов изомеризации к выходу продуктов дейтерирования, наблюдаемое при изомеризации октена-1 в CH3COOD, можно легко понять, если принять, что гидридный комплекс палладия, образующийся в первом периоде изомеризации олефина, изомеризует октен-1 быстрее по сравнению с изотопным обменом с растворителем. Небольшое количество дейтерия в образующихся олефинах обычно нельзя определить методом ИК-спектроскопии. [41]
Такая обобщенная качественная трактовка в общих чертах совпадает с точкой зрения Джибба [13] ( автор данной главы делает несколько меньший упор на вклад ионных структур в полный набор структур) и не противоречит установленным физическим свойствам соединений. Гидрид палладия отличается от гидридов переходных металлов начальных групп. Вызывает разногласия трактовка фазы PdH. Автор предпочитает рассматривать фазу PdH как нестехиометри-ческий гидрид и считает, что водород в этом соединении имеет значительно меньшую плотность отрицательного заряда, чем в гидридах группы титана и ванадия. [42]
Для того чтобы восстановление углекислоты протекало нормально, оно должно происходить в отсутствии как минеральных кислот, так и оснований. Я осуществил эти условия, применяя в качестве источника водорода in statu nascendi гидрид палладия. Действительно, при действии гидрида палладия на насыщенный раствор углекислоты в течение 30 дней я получил формальдегид, который мне удалось обнаружить в виде ангид-роформальдегиданилина и бромистого производного гексаметилентет-рамина. [43]
Катализаторами процесса, в основном, являются благородные металлы: родий, рутений и чаще всего палладий, нанесенные на тот или иной носитель. По нашему мнению, пал-ладиевый катализатор для реакции гидрирования бензойной кислоты является не самым удачным. В процессе гидрирования он очень быстро дезактивируется, что связано с образованием гидридов палладия и большими потерями металла с носителя. Поэтому кроме реактивации в последующих циклах гидрирования необходимо часть отработанного катализатора отбирать и заменять свежим. [44]
Для этого гипотетического соединения Нейс и Астон [56] предложили модель с атомами водорода в тетраэдрических пустотах; согласно более привлекательному варианту Астона и Митацека [60, 61], атомы водорода находятся в октаэдрических пустотах, а плоскости PdH4 и Pd чередуются. Ни одна из моделей не согласуется со всеми данными по структуре и составу гидридов палладия и не объясняет их полностью. При низкой температуре ( 4 2 К) атомы водорода в решетке гидрида палладия перемещаются в тетраэдрические пустоты, что сопровождается незначительным тригональным искажением решетки. Предполагалось, что такая миграция начинается при примерно 55 К и что ею объясняются наблюдаемые аномалии удельной теплоемкости и электросопротивления. [45]
Страницы: 1 2 3 4