Гидрид - ванадий
Cтраница 2
Уже предварительные исследования гидридов металлов методом ЯМР показали, что при комнатной температуре резонансные линии гидридов ванадия [38, 121] и тантала [51, 52] значительно уже, чем для гидридов титана и циркония. [16]
Оптимальные режимы получения гидридов таковы: выдержка от 45 мин до 1 ч и температура для гидрида титана - 675 - 800, для гидрида ванадия - 750 - 900, для гидрида ниобия - 675 - 800, для гидрида тантала - 740 - 835 С. [17]
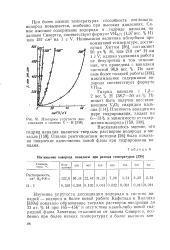 |
Изотермы упругости диссоциации в системе V - Н. [18] |
При более низких температурах способность поглощать водород повышается, особенно при высоких давлениях. Самое высокое содержание водорода в гидриде ванадия, по данным Сивертса, соответствует формуле VH0 7i ( 1 37 вес. [19]
Стационарные устройства для хранения водорода в форме гидридов не имеют строгих ограничений по массе и объему, поэтому лимитирующим фактором выбора того или иного гидрида будет, по всей вероятности, его стоимость. Для некоторых направлений использования может оказаться полезным гидрид ванадия, поскольку он хорошо диссоциирует при температуре, близкой к 270 К. Рвдрид магния является относительно недорогим, но имеет сравнительно высокую температуру диссоциации 560 - 570 К и высокую теплоту образования. Железо-титановый сплав сравнительно недорог, а гидрид его диссоциирует при температурах 320 - 370 К с низкой теплотой образования. Использование гидридов имеет значительные преимущества в отношении техники безопасности. Поврежденный сосуд с гидридом водорода представляет значительно меньшую опасность, чем поврежденный жидководородный танк или сосуд высокого давления, заполненный водородом. [20]
Если исходить из мольных долей, то больше всего водорода поглощают переходные элементы, расположенные в левой части периодической таблицы. Титан и цирконий дают нестехиометрические соединения, приближающиеся по составу к МН2, а гидриды ванадия и гафния приближаются к МН. Такая тенденция продолжается до платиновых металлов, которые, за исключением палладия, проявляют сравнительно небольшую способность реагировать с водородом, если не считать, что они могут поглощать некоторое количество водорода. [21]
Тем не менее на основании существующих данных можно сказать, что их структура более проста, чем структура гидридов ванадия. Методом ЯМР установлено [193], что атомы водорода при низких температурах занимают октаэдрические пустоты ( 1 / 21 / 20) и ( 001 / 2), согласно модели, предложенной Гиббом [54], Однако несколько лучшая степень согласия для теоретических и экспериментальных значений вторичных моментов линий ядерного магнитного резонанса показывает, что в этих, условиях более вероятно замещение тетраэдрических пустот ( 01 / 21 / 2) и ( 1 / 201 / 2), как это было предложено Хаггом [61 ] для гидрида тантала. [22]
Тем не менее на основании существующих данных можно сказать, что их структура более проста, чем структура гидридов ванадия. Однако несколько лучшая степень согласия для теоретических и экспериментальных значений вторичных моментов линий ядерного магнитного резонанса показывает, что в этих условиях более вероятно замещение тетраэдрических пустот ( О1 / 1 /) и ( VaO1 /), как это было предложено Хаггом [61 ] для гидрида тантала. [23]
Получение селенидов ванадия взаимодействием H2Se с порошкообразным металлическим ванадием затруднено вследствие образования гидридов ванадия. Кроме того, на поверхности ванадия в первый момент вследствие экзотермичности реакции образуется склонная к спеканию пленка селенида, через которую затруднено проникновение H2Se и Se, а также выделение водорода и разрушение гидрида ванадия. [24]
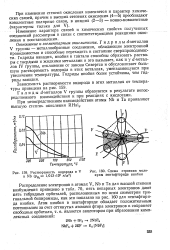 |
Растворимость водорода в V [ IMAGE ] Схема строения моле-и Nb ( Рн2 - 1 s H. MZ кулы пентафторида ниобия. [25] |
Гидриды d - металлов V группы - металлообразные соединения, обладающие электронной проводимостью и способные переходить в состояние сверхпроводимости. Гидриды ванадия, ниобия и тантала способны образовать растворы с твердыми и жидкими металлами и это вызывает, как и у d - металлов IV группы, отклонение от закона Сивертса и обусловливает большую растворимость водорода в этих металлах, уменьшающуюся при увеличении температуры. Гидриды ниобия более устойчивы, чем гидриды ванадия. [26]
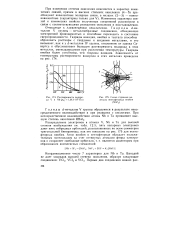 |
Растворимость водорода V и Nb ( pHi 1 013 - 105 Па.| Схема строения молекулы пентафторида ниобия ( NbF5. [27] |
Гидриды d - ме-таллов V группы - металлообразные соединения, обладающие электронной проводимостью и способные переходить в состояние сверхпроводимости. Гидриды ванадия, ниобия и тантала способны образовать растворы с твердыми и жидкими металлами, и это вызывает, как и у d - металлов IV группы, отклонение от закона Си-вертса и обусловливает большую растворимость водорода в этих металлах, уменьшающуюся при увеличении температуры. Гидриды ниобия более устойчивы, чем гидриды ванадия. [28]
 |
Растворимость водорода в V и Nb 0 н Х X 10 Па.| Схема строения молекулы пентафторида ниобия. [29] |
Гидриды d - метал-лов V группы - металлообразные соединения, обладающие электронной проводимостью и способные переходить в состояние сверхпроводимости. Гидриды ванадия, ниобия и тантала способны образовать растворы с твердыми и жидкими металлами и это вызывает, как и у d - металлов IV группы, отклонение от закона Сивертса и обусловливает большую растворимость водорода в этих металлах, уменьшающуюся при увеличении температуры. Гидриды ниобия более устойчивы, чем гидриды ванадия. [30]
Страницы: 1 2 3