Гидрид - уран
Cтраница 2
При взаимодействии гидрида урана с рассчитанными количествами аммиака или азота образуются нитриды урана. Светло-серый мононитрид урана устойчив до 1700 С, но подвержен воздействию воздуха и водяного пара. Соединения состава от U2Ns, разлагающегося ч вакууме при 700 - 800 С, до UN2, существующего при высоких давлениях азота, представляют собой монофазные твердые продукты. [16]
Упругость диссоциации гидрида урана в последней работе дана как функция состава твердой фазы и температуры. [17]
Щелочи с гидридом урана не реагируют. Энергично взаимодействует UH3 с органическими галогенидами, отнимая галоид; при этом образуется свободный углерод. Аммиак разлагает UHs при 250 с образованием нитрида. [18]
Оказывается, что гидрид урана легче всего образуется в местах нарушений кристаллической решетки, например на границах зерен или на границе раздела матрицы металла и какого-либо неметаллического включения. Во время выдержки в среде водорода такие гидридные включения могут расти в направлении этих нарушений и проникать вглубь от поверхности образца. [19]
И в то же время гидрид урана проявляет свойства металлического соединения, так как, например, электропроводность - величина того же порядка, что и электропроводность металлического урана. [20]
Азотная кислота бурно реагирует с гидридом урана, образуя уранил-нитрат. [21]
Для получения водорода термическим разложением используют гидриды урана, титана, реже гидрид циркония. На предварительной стадии гидрируют металл ( титан, цирконий, уран) неочищенным водородом с прочным связыванием всех его примесей. При разложении полученного гидрида водород начинает выделяться при сравнительно низких температурах: гидрид урана выделяет водород до 300 С, гидриды титана и циркония - в области температур 350 - 800 С. Примеси кислорода, азота, углерода и другие связываются металлом более прочно и при этих условиях не выделяются. [22]
По внешнему виду и физическим свойствам гидрид урана, коричневато-серый пирофорный порошок, напоминает металлоподобные гидриды лантана, церия и других редкоземельных металлов. [23]
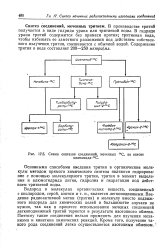 |
Схема синтезов соединений, меченных 14С, на основе. [24] |
В производстве тритий получается в виде гидрида урана или тритиевой воды. В гидриде урана тритий содержится без примеси протия; тритиевая вода, чтобы избежать ее заметного разложения под действием собственного излучения, трития, смешивается с обычной водой. Содержание трития в воде составляет 200 - 250 мкюри / мл. [25]
Тонкий порошок урана, получаемый диссоциацией гидрида урана, абсорбирует водород уже при температуре твердой углекислоты. [26]
При рассмотрении вопроса о химической природе гидрида урана и отклонения состава его от стехиометрического следует отметить теоретическую работу Либовица [224], в которой автор показывает, что большинство гидридов переходных металлов не отвечает целому и кратному отношению компонентов и характеризуется недостаточностью водорода. Это объясняется тем, что они являются фазами внедрения или твердыми растворами водорода в металле с водородом, расположенным в промежутках решетки металла. [27]
По данным работы Тржебятовского и других [239], гидрид урана ниже 173 К обладает ферромагнитными свойствами. [28]
Очень чистый сухой водород может быть получен термическим разложением гидрида урана. Гидрид же может быть-приготовлен из металлического урана и водорода, не подвергнутого тщательной, очистке. [29]
Восстановление безводного тетрафторида урана атомарным водородом и реакция между гидридом урана и фтористым водородом приводят к образованию трифторида урана. Производными соединениями от него яляются псевдотрифториды PbUFe, SrUF6 и BaUFe, которые могут быть осаждены из растворов, содержащих одинаковые количества двух - и четырехвалентных ионов. Эти соединения аналогичны вышеописанным смешанным фторидам тория. О конце реакции судят по образованию значительных количеств гексафторида, который удаляют отгонкой в вакууме. [30]
Страницы: 1 2 3 4