Гидрид - элемент - подгруппа
Cтраница 2
Вследствие слабости электронодо-норных свойств гидриды элементов подгруппы мышьяка основными свойствами не обладают. [16]
Наиболее применима ид-система к гидридам элементов подгрупп IA, ПА, VIA и VIIA: характер заряда водорода в этих гидридах известен. [17]
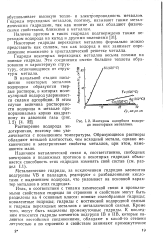 |
Изотермы адсорбции водорода некоторыми металлами. [18] |
Металлические гидриды, за исключением гидридов элементов подгруппы VB и палладия, реагируют с разбавленными кислотами с выделением водорода, что указывает на основной характер металлов в этих гидридах. [19]
Для алкилгидридов, получаемых замещением водорода в гидридах элементов подгруппы III А, также сохраняется строение исходных гидридов, например для диборана возможно замещение только 4 атомов водорода органическими радикалами; максимальное алкилирование дает соединение с общей формулой B2H2R4 - Водородный мостик при этом сохраняется. Гидриды алкилалюми-ния также ассоциированы. [20]
Особое место отводится водородной связи в объяснении строения гидридов элементов подгруппы IIIA. В этих гидридах не выполняется закон валентности, согласно которому каждая ковалент-ная связь осуществляется обобществленной парой электронов. Однако такие соединения экспериментально не получены: они существуют только в виде димеров и более крупных ассоциатов-полимеров, например, В2Н6, ( А1Н3) Ж, где элементы подгруппы IIIA выступают формально как четырехвалентные. В многоатомных молекулах гидридов бора ( В4Ню, BsHg, ВюНн и другие) бор также имеет необычную валентность. [21]
В отличие от гидридов щелочных и щелочноземельных элементов, гидриды элементов подгруппы IIIA не могут быть получены прямым синтезом из элементов. [22]
В отличие от гидридов элементов VII и VI групп гидриды элементов подгруппы азота проявляют не кислотные, а слабые основные свойства. [23]
В табл. Ill, 1 приведены энтропии 298 и их разности для гало-генидов и гидридов элементов подгруппы лития в газообразном состоянии. [24]
В табл. Ill, 1 приведены энтропии Sags и их разности для гало-генидов и гидридов элементов подгруппы лития в газообразном-состоянии. [25]
Простые и некоторые сложные гидриды элементов V и VI групп, кроме упомянутых выше комплексов с гидридами элементов подгруппы III А, образуют многочисленные комплексы с разнообразными соединениями. [26]
Как и в других соединениях, ковалентная связь в гидридах обладает большой энергией - - 60 - 140 ккал / моль, уменьшающейся ( в одной и той же группе) с увеличением атомного веса элемента. Гидриды элементов подгрупп IVA-VIIA обладают свойствами, присущими соединениям с ковалентной связью: низкомолекулярные соединения газообразны или легко летучи; обладают высокой термической стабильностью от 400 до 1000 С и более; не проводят электрический ток; в большинстве случаев хорошо растворимы. В твердом состоянии эти гидриды имеют молекулярную решетку; в газообразном - молекулы не ассоциированы. [27]
Некоторые гидриды элементов подгрупп VII и VIA при присоединении к ним протона образуют комплексные гидрид-катионы. [28]
Гидриды данных металлов получают нагреванием простых веществ в атмосфере водорода. Известны и другие гидриды элементов подгруппы скандия, которые относятся к фазам внедрения. Гидриды - твердые вещества серого или черного цвета, электропроводны. [29]
В отношении строения и природы химической связи различные гидриды изучены не одинаково. Наиболее исследовано строение гидридов элементов подгруппы IVA, которое хорошо объясняется представлениями ковалентной связи. [30]
Страницы: 1 2 3