Гидрид - элемент - группа
Cтраница 1
Гидриды элементов V группы: фосфин, арсин и стибин являются легковоспламеняющимися веществами. Хотя чистые гидриды в смеси с воздухом не способны к самопроизвольному воспламенению, при наличии в них примесей, в частности высших гидридов, такое воспламенение может произойти. Поэтому все работы с этими гидридами следует проводить в аппаратуре, тщательно освобожденной от воздуха. Особую опасность представляют осадки высших гидридов, иногда отлагающиеся на стенках аппаратуры и в других местах при работе с фосфином. [1]
Для гидридов элементов VII группы ( галоиды), несмотря на их явно кислотный характер, удалось найти условия, при которых водород способен отрываться в виде гидрид-иона. [2]
Взаимодействие с гидридами элементов группы ША происходит, по-видимому, по электрофильному механизму ( или по четырехцентровому перициклическому с некоторыми чертами электрофильного), тогда как для гидридов элементов группы IVA более вероятен механизм с участием свободных радикалов. [3]
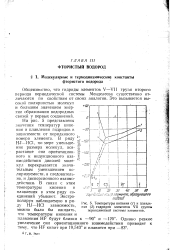 |
Температуры кипения ( 1 и плавле. [4] |
Общеизвестно, что гидриды элементов V-VII групп второго периода периодической системы Менделеева существенно отличаются по свойствам от своих аналогов. Это вызывается высокой полярностью молекул и большим значением энергии образования водородных связей у первых соединений. [5]
По глубокой очистке гидридов элементов VI группы известно мало работ. [6]
Сравнение энергий образования гидридов элементов VI группы указывает на падение прочности связи при переходе от О к Ро, что и естественно как нормальный ход в отсутствие усложняющих эффектов повышения валентного состояния. Такое усложнение наблюдается в случае окислов. [7]
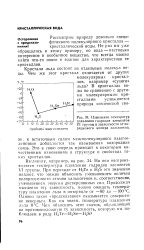 |
Изменение температур плавления гидридов элементов VI группы в зависимости от порядкового номера халькогена. [8] |
На нем воспроизводятся температуры плавления гидридов элементов VI группы. При переходе от Н2Те к Й25 эти значения падают, что можно объяснить уменьшением величин поляризуемости атомов халькогенов и, соответственно, уменьшением энергии дисперсионных сил. [9]
По отношению к кислороду реакционноспособность гидридов элементов V группы растет от аммиака к висмутину. Все гидриды являются восстановителями, причем последние члены ряда более сильные, чем аммиак. [10]
 |
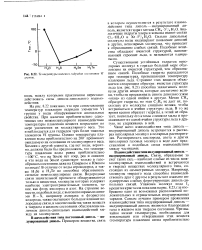
Зависимость концентрации хлорида галлия ( C ( ja в ПГС от линейной скорости газового потока при 800 ( 1, 700 ( 2 и 600 С. [11] |
Однако к недостаткам ее относится необходимость употреблять сильно токсичные гидриды элементов V группы. [12]
 |
Температуры кипения гидридов элементов VI группы. [13] |
На рис. 8.22 показано, что при сопоставлении температур плавления гидридов элементов VI группы у воды обнаруживаются аномальные свойства. При наличии приблизительно однотипных сил межмолекулярного взаимодействия температуры плавления веществ возрастают по мере увеличения их молекулярного веса. Это и наблюдается для гидридов трех более тяжелых элементов VI группы. Однако температура плавления воды приблизительно на 200 превышает ожидаемую на основании ее молекулярного веса. Химики с другой планеты, где нет воды, вероятно, должны были бы предположить, что температура плавления воды равна приблизительно - 100 С, что на Земле нет озер, рек и океанов и что вода на Земле существует только в газообразном состоянии даже на Северном и Южном полюсах. В отличие от воды сероводород, а также H2Se и Н2Те не способны образовывать сильные межмолекулярные связи. Водородные связи значительной прочности обнаруживаются только в веществах, молекулы которых содержат наиболее электроотрицательные элементы, такие, как фтор, кислород и азот. На строение веществ, подобных воде, с высокополярными связями Н - X, например аммиака и фтористого водорода, также оказывают большое влияние водородные связи, и многие свойства таких веществ в твердом и жидком состояниях обусловлены наличием диполь-дипольных взаимодействий между их молекулами. [14]
Вычисление относительных вероятностей перехода для некоторых систем полос окислов и гидридов элементов II группы. [15]
Страницы: 1 2