Рассматриваемый гидрид
Cтраница 1
Рассматриваемые гидриды, особенно AsHs, являются сильнейшими неорганическими ядами. Это относится и ко всем летучим, и к растворимым соединениям мышьяка. [1]
 |
Структура димерной молекулы As4O6. [2] |
Рассматриваемые гидриды, особенно AsH3, являются сильнейшими неорганическими ядами. Это относится и ко всем летучим и растворимым соединениям мышьяка. [3]
Рассматриваемые гидриды, особенно AsH3, являются сильнейшими неорганическими ядами. Это относится и ко всем летучим, и к растворимым соединениям мышьяка. [4]
Рассматриваемые гидриды легко образуют комплексы с донорами электронов: известны многочисленные комплексы, в которых группы ВН3, А1Н3, GaH3 связаны с аминами, фосфинами, эфи-рами, сульфидами и другими лигандами. [5]
Прочность рассматриваемых гидридов максимальна у гидридов бора. Диборан стоек до - 100 С; при более высоких температурах наблюдается частичное отщепление водорода с образованием бороводородов с большим молекулярным весом, из которых пента - и декаборан выдерживают нагревание до 120 и 200 С. Еще более стойки некоторые производные бороводородов, которые выдерживают температуру 500 С и выше. Для полного разложения диборана на элементы требуется нагревание до 700 - 800 С, гидрид алюминия разлагается уже при 100 С; гидрид галлия при 35 С, а гидриды индия и таллия - при комнатной температуре. Прочность гидридов значительно повышается при образовании комплексов и особенно двойных гидридов. [6]
Металлические свойства рассматриваемых гидридов возникают в результате свободно перемещающихся в кристаллической решетке электронов, оставшихся после образования связи. Например, если в гидриде состава МНИ у металла m валентных электронов, а участвует в связях только пгГ - ионов, то разность ( т - п) даст число электронов, вызывающих металлические свойства. Когда т л, то металлические свойства исчезают и гидриды будут ионными. [7]
Солеобразная природа рассматриваемых гидридов была также непосредственно доказана выделением водорода при электролизе расплавленного LiH на аноде. [8]
По химическим свойствам рассматриваемые гидриды близки гидридам щелочных металлов, но менее активны. Это вызвано, помимо всего прочего, тем, что на поверхности гидрида отлагаются продукты реакции, зачастую нерастворимые в реагенте ( например, HzO), препятствующие контакту гидрида с реагентом. Наиболее подробно изучен гидрид кальция; гидриды стронция и бария исследованы меньше, так что трудно сделать определенный вывод о том, имеются ли существенные различия-между ними и гидридом кальция. Возможно, гидрид бария несколько более активен, чем гидриды кальция и стронция. [9]
По составу и физическим свойствам рассматриваемые гидриды напоминают соли галоводородных кислот. Потому их называют со-леобразными гидридами. Они представляют собой кристаллические вещества, довольно тугоплавкие. [10]
Важнейшими физическими свойствами, изучение которых способствовало пониманию строения рассматриваемых гидридов, являются их электрические и магнитные свойства. [11]
Важнейшими физическими свойствами, изучение которых способствовало пониманию строения рассматриваемых гидридов, являются их электрические и магнитные свойства. [12]
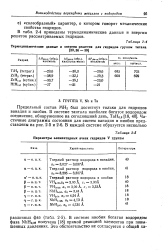 |
Параметры элементарных ячеек гидридов V группы. [13] |
В табл. 2 - 4 приведены термодинамические данные и энергии решеток рассматриваемых гидридов. [14]
Аналогичные производные золота не получены. Устойчивость рассматриваемых гидридов может быть иногда сильно повышена комплексообразова-нием. [15]
Страницы: 1 2