Рассматриваемый гидрид
Cтраница 2
В настоящее время известны гидрид-анионы для бора, алюминия, галлия и индия. Катионами в рассматриваемых гидридах могут быть все элементы подгрупп IA, ПА, IIIA. Из элементов подгруппы IB в комплексные гидриды входит медь и серебро, из элементов подгруппы ПВ - цинк и кадмий. Многие лантаноиды также входят в комплексные гидриды. [16]
 |
Строение молекул галогеноводородов. [17] |
Значит, у теллуристого водорода две связи с водородом образуют два чистых электронных р-облака атома теллура, ориентированные под прямым углом. У селено - и сероводорода примесь s - состояния также незначительна, из-за чего валентные углы мало отличаются от прямого. Кроме того, в ряду рассматриваемых гидридов прочность связей Э - Н закономерно падает. [18]
Гидриды лития и его аналогов ( ЭН) образуются при пропускании сухого водорода над нагретым металлом. По внешнему виду и большинству физических свойств гидриды похожи на соответствующие галоидные соли. Так, лучше других изученный LiH образует твердые бесцветные кристаллы, в отсутствие воздуха плавящиеся без разложения при 668 С. Солеобразная природа рассматриваемых гидридов была также непосредственно доказана выделением водорода при электролизе расплавленного LiH на аноде. [19]
Гидриды лития и его аналогов ( ЭН) образуются при пропускании сухого водорода над нагретым металлом. По внешнему виду и большинству физических свойств гидриды похожи на соответствующие галоидные соли. Так, лучше других изученный LiH образует твердые бесцветные кристаллы, в отсутствие воздуха плавящиеся без разложения при 668 С. Солеобразная природа рассматриваемых гидридов была также непосредственно доказана выделением водорода при электролизе расплавленного LiH на аноде. [20]
Комплексообразование и особенно образование двойных гидридов приводят к значительному повышению стойкости по отношению к воде и другим нуклеофильным реагентам. Однако алюмогидриды этих металлов легко разлагаются водой. Другим характерным свойством рассматриваемых гидридов является высокая восстанавливающая способность по отношению ко многим неорганическим и органическим соединениям. Наконец, у гидридов элементов подгруппы IIIA более, чем у элементов других групп, выражена склонность к присоединению по двойной связи к непредельным соединениям. [21]
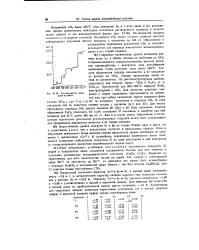 |
Растворимость водорода в уране. [22] |
Для нептуния, плутония, америция и кюрия характерны образующиеся из элементов уже при слабом нагревании черные гидридные фазы состава ЭН2, где О sg x 0 7, но возможно получение и гидридов ЭНз. В этом отношении они до известной степени сходны с лантаном ( § 5 доп. Для теплот образования гидридов ЭН2 даются значения 28 ( Np) и 40 ( Am) ккал / моль. Теплота образования PuHj ( плотность 9 6 г / сж3) составляет 37 ккал / моль, а давление над ним водорода при 25 С равно 350 мм рт. ст. Как и в случае урана, образование и последующее термическое разложение рассматриваемых гидридов может быть использовано для превращения компактных металлов в их тонкие порошки. [23]
Взаимодействие водорода с нагретыми щелочными металлами идет медленнее, чем с щелочноземельными. В случае Li требуется нагревание до 700 - 800 С, тогда как его аналоги взаимодействуют уже при 350 - 400 С. Для достижения наибольшей полноты использования металла целесообразно вводить в реакционное пространство его пары. Можно также воспользоваться тем, что при нагревании в атмосфере водорода образующийся гидрид возгоняется ( хотя и с трудом) и оседает затем на более холодных частях реакционного сосуда в виде бесцветных игол или похожей на вату спутанной кристаллической массы. Интересным способом образования рассматриваемых гидридов ( наряду с окислами ЭцО) является взаимодействие щелочного металла с его расплавленной гидроокисью ( доп. [24]
Взаимодействие содорода с нагретыми щелочными металлами идет медленнее, чем с щелочноземельными. В случае Li требуется нагревание до 700 - 800 С, тогда как его аналоги взаимодействуют уже при 350 - 400 С. Для достижения наибольшей полноты использования металла целесообразно вводить в реакционное пространство его пары. Можно также воспользоваться тем, что при нагревании в атмосфере водорода образующийся гидрид возгоняется ( хотя и с трудом) и оседает затем на более холодных частях реакционного сосуда в виде бесцветных игол или похожей на вату спутанной кристаллической массы. Интересным способом образования рассматриваемых гидридов ( наряду с окислами ЭгО) является взаимодействие щелочного металла с его расплавленной гидроокисью ( доп. [25]
Страницы: 1 2