Двухатомный гидрид
Cтраница 1
Двухатомные гидриды, как, например, ВЫ, СН, NH и ОН, так же как LiH, NaH, CaH и А1Н и более известные химически устойчивые гидриды HF, НС1, НВг и HJ, представляют особый интерес потому, что они являются, вероятно, единственной группой молекул, которые по структуре приближаются к объединенному атому, если не считать самого молекулярного водорода. Для иллюстрации методов изучения электронных структур и состояний двухатомных гидридов будет выбран радикал СН, о котором имеется много спектроскопических данных. Объединенным атомом, соответствующим СН, является атом азота; он имеет основное 5ц - состояние, а также Юм - и 2Рц - состояния, обладающие несколько большими энергиями. [1]
Величины Z / Z для двухатомных гидридов в функции от порядкового номера элемента образуют периодическую кривую с максимумами для гидридов галоидов и минимумами для гидридов щелочных металлов. Для обмена между ними коэффициент обмена больше всего отличается от единицы. [2]
Специфическую картину представляет собой сопоставление двухатомных гидридов элементов II периода. Особенностью их является то, что во всем ряду от Li до F эти молекулы по числу электронов не превосходят восьми. Таким образом, поворота гомопериодной линии, зависящего от накопления электронов свыше десяти, быть не может, и линия остается более или менее монотонной, причем ДЯ образования растет от LiH к HF. В табл. 73 даны значения длин связей и энергий диссоциации, двухатомных гидридов на атомы. [3]
В табл. 34 приведены экспериментальные характеристики двухатомных гидридов элементов разной валентности. [4]
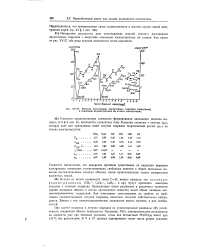 |
Энергии диссоциации двухатомных гидридов ( ккал / моль и ионизации иэоэлектронных им атомов ( ккал / г-атом. [5] |
Интересные результаты дает сопоставление энергий ( теплот) диссоциации двухатомных гидридов с энергиями ионизации изоэлектронных им атомов. Как видно из рис. XV-27, оба ряда величин изменяются почти однотипно. [6]
Для наглядности мы сопоставляем прежде всего на одном чертеже ( рис. 196) схемы энергетических уровней для всего ряда двухатомных гидридов; на каждом уровне, кроме его символа, указана численно и заселенность его электронами. Уровни, играющие наиболее важную роль в упрочнении связей, отмечены жирной черточкой; незанятые в основном состоянии атома уровни обозначены пунктиром, и, естественно, на них не указана заселенность. Положение атомных уровней IsH отмечено весьма приближенно волнистыми линиями. [7]
Чтобы установить, какую ошибку вносит при расчетах по каждой из этих формул пренебрежение вкладами, возникающими благодаря смещению электронной плотности от ядра, в работе [14] также произведено сопоставление градиентов электрического поля qD широкого ряда двухатомных гидридов элементов 2-го и 3-го периодов с экспериментальными значениями К. [8]
Колебательные постоянные SH в Х2Пгсостоянии, приведенные в табл. 78, как уже указывалось, приняты по данным Лича [2574], а вращательные постоянные Ве и ах вычислены Хачкурузовым [441 ] по данным работ [3356] и [2574] с учетом корреляции значений молекулярных постоянных двухатомных гидридов и дейте-ридов элементов второго и третьего периодов таблицы Менделеева. [9]
Это иллюстрируется кривой потенциальной энергии молекулы ВеН, представленной на рис. 5.6. Здесь, так же, как на рис. 5.2, учтено правило непересечения. Среди двухатомных гидридов, образованных атомами второго периода ( от LiH до HF), ВеН имеет самую низкую энергию диссоциации, так как только для Be требуется возбудить атом, прежде чем электроны станут способными к образованию связи. [10]
Ранее высказывалось предположение, что, если энергия; переходящая в поступательное движение, превышает 50 см 1, перекрывание поступательных волновых функций или туннельный переход между поверхностями потенциальной энергии становится малым. При изучении вращательной релаксации электронно-возбужденных двухатомных гидридов получены подтверждения этого предположения. Бреннен и Каррингтон [174] доказали справедливость правила А / 1 в процессе вращательной релаксации радикалов СН при столкновениях с атомами инертных газов. [11]
В настоящее время наука уже обладает сводной характеристикой двухатомных гомонуклеарных молекул для ряда от Li2 до Ne2; к сожалению, таких полных сведений для ряда от Na2 до Аг2 еще не имеется и это лишает возможности провести более полное сравнение кайносимметриков 2р с Зр-элементами. Подобное сравнение возможно пока только для двухатомных гидридов элементов 2-го и 3-го периодов. [12]
Двухатомные гидриды, как, например, ВЫ, СН, NH и ОН, так же как LiH, NaH, CaH и А1Н и более известные химически устойчивые гидриды HF, НС1, НВг и HJ, представляют особый интерес потому, что они являются, вероятно, единственной группой молекул, которые по структуре приближаются к объединенному атому, если не считать самого молекулярного водорода. Для иллюстрации методов изучения электронных структур и состояний двухатомных гидридов будет выбран радикал СН, о котором имеется много спектроскопических данных. Объединенным атомом, соответствующим СН, является атом азота; он имеет основное 5ц - состояние, а также Юм - и 2Рц - состояния, обладающие несколько большими энергиями. [13]
В спектрах этих пламен наблюдаются три системы полос СН, начинающиеся примерно при одной длине волны. Системы полос имеют разрешенную вращательную структуру, характерную для спектров двухатомных гидридов, и дуплетные ветви, показывающие, что молекула-излучатель имеет нечетное число электронов. Поскольку аналогичные полосы легко получить в условиях разря-да в парах чистых углеводородов, излучателем полос может быть только радикал СП. [14]
Однако среди них не встречаются соединения со стехиометрическим составом. Как показывают исследования линейных спектров, в пламени и в дуге существуют многочисленные двухатомные гидриды. Большинство из них, например СН, NH, ОН, MgH, ZnH, АШ, AuH, при нормальных условиях или неустойчивы, или не образуются в весомых количествах. [15]
Страницы: 1 2