Поверхностный гидрид
Cтраница 1
Поверхностные гидриды и нитриды образуются легче, чем соответствующие объемные фазы. Это можно объяснить тем, что положение поверхностных атомов металла менее фиксировано, чем положение атомов в объеме, что облегчает внедрение атомов газа. [1]
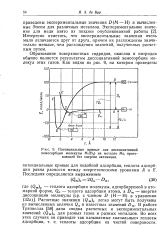 |
Потенциальные кривые для диссоциативной. [2] |
Образование поверхностных гидридов, окислов и нитридов обычно является результатом диссоциативной хемосорбции молекул этих газов. [3]
Образование такого типа поверхностных гидридов приводит к активации водорода, необходимой для дальнейшего развития процесса восстановления. [4]
Катализаторы этих реакций образуют нестойкие поверхностные гидриды. Металлы переходной и платиновой групп ( Ni, Fe, Co и Pt) могут оказаться пригодными аналогично окислам или сульфидам металлов переходной группы. Данный тип реакций является чрезвычайно важным: он включает такие процессы, как синтез аммиака и метанола, реакцию Фишера - Тропша, оксо-синтез, синтол-процесс, а также получение спиртов, альдегидов, кетонов, аминов и пищевых жиров. [5]
Катализаторы этих реакций образуют нестойкие поверхностные гидриды. Металлы переходной и платиновой групп ( Ni, Fe, Co и Pt) могут оказаться пригодными аналогично окислам или сульфидам металлов переходной группы. Данный тип реакций является чрезвычайно важным: он включает такие процессы, как синтез аммиака и метанола, реакцию Фишера-Тропша, оксо-синтез, синтол-процесс, а также получение спиртов, альдегидов, кетонов, аминов и пищевых жиров. [6]
Катализаторы этих реакций образуют нестойкие поверхностные гидриды. Металлы переходной и платиновой групп ( Ni, Fe, Co и Pt) могут оказаться пригодными аналогично окислам или сульфидам металлов переходной группы. Данный тип реакций является чрезвычайно важным: он включает такие процессы, как синтез аммиака и метанола, реакцию Фишера - Тропша, оксо-синтез, синто л-процесс, а также получение спиртов, альдегидов, кетонов, аминов и пищевых жиров. [7]
Катализаторы этих реакций образуют нестойкие поверхностные гидриды. Металлы переходной и платиновой групп ( Ni, Fe, Co и Pt) могут оказаться пригодными аналогично окислам или сульфидам металлов переходной группы. Данный тип реакций является чрезвычайно важным: он включает такие процессы, как синтез аммиака и метанола, реакцию Фишера-Тропша, оксо-синтез, синтол-прбцесс, а также получение спиртов, альдегидов, кетонов, аминов и пищевых жиров. [8]
Трудность в определении образования поверхностных гидридов состоит в том, что водород почти всегда содержится в объеме углей. Если водород присутствует в небольшом количестве, то его трудно определить с достаточной точностью. Необходимо использовать точные аналитические методы при измерении поглощения водорода углями, приготовленными при тщательном удалении содержащих водород примесей. [9]
 |
Схема, поясняющая причину появления. [10] |
Так, на модели рис. 2 поверхностный гидрид ( или хемосорбированный водород) характеризуется положением атома водорода в ямке М, окруженной тремя атомами катализатора, тогда как при гидрогенизации активен атом водорода, расположенный в ложбине только между двумя соприкасающимися атомами катализатора. [11]
В этих опытах не было обнаружено образование поверхностного гидрида. Однако графой не очень пригоден для этих экспериментов из-за однородности его поверхности, которая почти целиком состоит из базисных плоскостей. [12]
При разряде протона на поверхности металла ( Мс) адсорбируется водород н образуется поверхностный гидрид МеН, где связь Мс - Н ковалентна. С увеличением потенциала Me эта связь ионизируется, и в переходном состоянии при реакции с окислителем водород ведет себя как гидрид-ион, причем перенапряжение дезактивирует восстанавливающее действие водорода. Восстановлению подвергается сопряженная к-та ( I) карбонильного соединения, к-рая образуется в результате присоединения протона по карбонильной группе. [13]
При разряде протона на поверхности металла ( Me) адсорбируется водород и образуется поверхностный гидрид МеН, где связь Me - Н ковалентна. С увеличением потенциала Me эта связь ионизируется, и в переходном состоянии при реакции с окислителем водород ведет себя как гидрид-ион, причем перенапряжение дезактивирует восстанавливающее действие водорода. Восстановлению подвергается сопряженная к-та ( I) карбонильного соединения, к-рая образуется в результате присоединения протона по карбонильной группе. [14]
С повышением температуры рекомбинация атомов водорода усиливается и часть поверхности металла, свободная от поверхностного гидрида, увеличивается. Это ведет к повышению обратимой молекулярной хемосорбции водорода. Сочетание атомарной и молекулярной хемоеорбции, увеличение доля молекулярной хемосорбции по мере возрастания температуры и является причиной увеличения суммарной адсорбции с повышением температуры. [15]
Страницы: 1 2