Поверхностный гидрид
Cтраница 2
По мере дальнейшего легирования начинает сказываться участие самих примесных атомов в хемосорбции с образованием поверхностных гидридов металлов, т.е. все в большей и большей степени начинают проявляться микрохимические свойства примеси, т.е. локальный эффект. [16]
Продукты базисной реакции ( Н 4 - Н 4 - е), адсорбированные на никеле, образуют метастабильный поверхностный гидрид NiH2 с металлической и ионной связью. Продолжительность образования на катализаторе ( Н 4 - Н 4 - е) адс соответствует индукционному периоду процесса, продолжительность которого зависит от концентрации компонентов и условий. [17]
При такой адсорбции молекулы водорода и кислорода распадаются на отдельные атомы, которые присоединяются к активной поверхности угля, образуя поверхностный гидрид и поверхностные окислы. [18]
Ион водорода в растворе вначале адсорбируется на электроде, далее дегидратируется и после самого электрохимического процесса разряда переходит в состояние поверхностного гидрида или адсорбционного соединения. Иногда он образует твердый раствор с металлом электрода. Вероятно, формы связи водорода на различных металлах неодинаковы. [19]
Адсорбция металлами и телами с весьма развитой поверхностью водорода не в виде молекул, а в виде атомов, вызывает к жизни теорию, что активность катализаторов в указанных процессах определяется способностью поглощать большие или меньшие количества атомарного водорода с образованием промежуточных поверхностных гидридов. Будучи весьма нестойкими, указанные гидриды должны разлагаться на свободный катализатор ( металл) и активно действующий атомарный водород. [20]
Расположение катализаторов по активности непосредственно определяется величиной предэкспоненциального множителя в уравнении скорости реакции. Исключительно низкую активность палладия следует объяснить образованием поверхностного гидрида. [21]
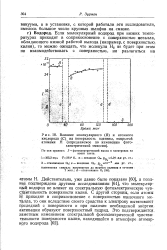 |
Влияние молекулярного ( В и атомного кислорода ( С на поверхность платины, покрытой атомами Н ( определяемое по изменению фотоэлектрической эмиссии. [22] |
Действительно, уже давно было показано [60], а позднее подтверждено другими исследованиями [ 61J, что молекуляр-щлй водород не влияет на спектральную фотоэлектрическую чувствительность поверхности калия. С другой стороны, если атомы Н приходят в соприкосновение с поверхностью щелочного ме-тдлла, то они вследствие своего сродства к электрону вытягивают последний с поверхности и при наличии необходимой энергии активации образуют поверхностный гидрид. [23]
Предположение о природе разрушения, выдвинутое в настоящей работе, состоит в том, что микротрещины в зоне сварного шва при сварке сплава Ti - 5А1 - 2 5Sn ( пч) с титаном Т1 - 55А являются отправными пунктами для начала образования гидрида титана. Микротрещины в поверхностном слое окисла титана вызваны, вероятно, термическими напряжениями при сварке и циклической сменой давления при изготовлении баков. В этом случае водород вступает в реакцию с высокоактивной поверхностью титана под микротрещиной и образует поверхностный гидрид титана. Поскольку гидрид титана очень хрупок, он будет растрескиваться под действием термических напряжений и циклического давления, образуя новые поверхности для воздействия водорода. В итоге образование гидрида вызывает растрескивание металла и его разрушение. [24]
Прилипание к поверхности часто сопровождается химической реакцией. На этом, в частности, основан метод плазменной пассивации поверхности металлов, когда металл при взаимодействии с атомами азота покрывается пленкой инертного нитрида металла. При взаимодействии Н2 с поверхностью металлов - - катализаторов гидрирования - Ni, Pt, Pd происходит разрыв Н - Н - связи и образование поверхностных гидридов металлов. Прилипание к поверхности жидкости сопровождается растворением в ней и возможными химическими реакциями в объеме жидкой фазы. [25]
Страницы: 1 2