Летучий гидрид
Cтраница 1
Летучие гидриды включают в себя обширную группу бинарных соединений элементов с водородом, и из всех гидридов имеют наибольшее практическое значение. Некоторые представители этой группы гидридов ( вода, углеводороды) весьма распространены в природе. [1]
Летучие гидриды образуют элементы IV, V, VI и VII групп периодической таблицы ( за исключением подгруппы А), а также бор. [2]
Мономерные летучие гидриды элементов подгрупп IIIА и VIA, за исключением метана, фосфина и сероводорода, в интервале температур 300 - 1300 К должны полностью разлагаться на элемент и водород, что и подтверждается на практике. Для полного разложения метана, фосфина и сероводорода требуются более высокие температуры. [3]
Характеристическим летучим гидридом углерода является метан. [4]
Характеристическим летучим гидридом углерода является метан. В обычных условиях водород с углеродом не реагирует. Применяются также и другие способы получения метана из сложных органических веществ. В лаборатории метан можно получить разложением карбида алюминия водой. В природе метан постоянно образуется при разложении органических веществ без доступа воздуха. Химическое строение метана определяется s / r - гибриди-зацией атома углерода. Молекула метана представляет собой правильный тетраэдр, в центре которого находится атом углерода, а по вершинам - атомы водорода. [5]
Характеристическим летучим гидридом углерода является метан. [6]
Многие летучие гидриды, молекулы которых имеют электронную оболочку, аналогичную оболочке атомов благородных газов ( как, например, сероводород), образуют ряд молекулярных соединений с неорганическими и органическими веществами. [7]
Образующие типичные летучие гидриды элементы 14 - 17 рядов и их аналоги из малых периодов в твердом состоянии практически не растворяют водород, а иногда непосредственно с ним и не соединяются. Однако будучи получены, гидриды этих элементов более или менее устойчивы. [8]
Кроме солеобразных и летучих гидридов, водород образует с элементами и другие группы соединений. К ним относятся полимерные, металлообразные и переходные гидриды. [9]
Олово образует летучий гидрид; однако при катодной поляри-ации последний выделяется только при повышенных плотностях ока, аналогично тому, как это происходит в случае свинца. Кор-озия наблюдается в кислых, нейтральных и щелочных растворах. [10]
Олово образует летучий гидрид; однако при катодной поляри-ации последний выделяется только при повышенных плотностях ока, аналогично тому, как это происходит в случае свинца. Кор-озия наблюдается в кислых, нейтральных и щелочных растворах. [11]
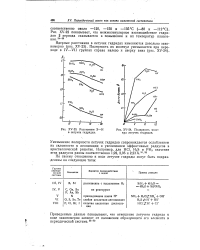 |
Расстояния Э - И в летучих гидридах. [12] |
Уменьшение полярности летучих гидридов сопровождается ослаблением их склонности к ассоциации и увеличением эффективных радиусов в кристаллической решетке. [13]
Уменьшение полярности летучих гидридов сопровождается ослаблением их склонности к ассоциации и увеличением эффективных радиусов в кристаллической решетке. Например, для НС1, H2S и РН3 значения этих радиусов равны соответственно 1 92, 2 05 и 2 23 А. [14]
Страницы: 1 2 3 4