Летучий гидрид
Cтраница 2
Газохроматографический анализ летучих гидридов не вызывает особых затруднений, несмотря на чрезвычайно высокую реакционную способность некоторых из них. Тем не менее при анализе гидридов металлов методом газовой хроматографии следует учитывать легкую окисляемость гидридов и ярко выраженную склонность к гидролизу. Из летучих гидридов сравнительно медленно разлагаются водой лишь гидриды Ge, Sn, P, As и Sb. Особенно большая осторожность необходима при анализе боранов. [16]
Газохроматографический анализ летучих гидридов не вызывает особых затруднений, несмотря на чрезвычайно высокую реакционную способность некоторых из них. Тем не менее при анализе гидридов металлов методом газовой хроматографии следует учитывать легкую окис-ляемость гидридов и ярко выраженную склонность к гидролизу. Из летучих гидридов сравнительно медленно разлагаются водой лишь гидриды Ge, Sn, P, As и Sb. Особенно большая осторожность необходима при анализе боранов. При этом недопустимо присутствие в хрома-тографической системе даже следов влаги или кислорода. Бор может образовывать с водородом цепочки, содержащие до 10 атомов бора. [17]
При этом образуются летучие гидриды. [18]
В случае самовоспламенения летучего гидрида из-за разгерметизации аппаратуры следует прежде всего устранить возможность утечки, перекрыв отдельные участки технологической системы, а затем приступить к тушению пламени. [19]
 |
Закон смещения г. [20] |
Характерная для ряда летучих гидридов ассоциация их молекул происходит в основном за счет образования водородных связей ( IV § 3 доп. В случае кислородных производных несимметричная водородная связь О - Н - О ( иногда называемая гидроксильной) обычно имеет длину около 2 75 А, а симметричная О Н О - около 2 5 А. [21]
Характерная для ряда летучих гидридов ассоциация их молекул происходит в основном за счет образования водородных связей ( IV § 3 доп. В случае кислородных производных несимметричная водородная связь О - - Н 0 ( иногда называемая г и д р о к с и л ь н о й) обычно имеет длину около 2 75 А, а симметричная О-Н-0 - около 2 5 А. [22]
Характерная для ряда летучих гидридов ассоциация их молекул происходит в основном за счет образования водородных связей ( IV § 3 доп. В случае кислородных производных несимметричная водородная связь О - Н - - - О ( иногда называемая гидроксильной) обычно имеет длину около 275 пм, а симметричная О - - Н - - О - около 250 пм. Несимметричные водородные связи встречаются гораздо чаще, чем симметричные. Хорошим примером последних может служить связь в ионе HFT ( VII § 1 доп. [23]
Константа диссоциации большинства летучих гидридов имеет высокое значение, что указывает на термодинамическую неустойчивость последних. Иная зависимость наблюдается для метана и сероводорода, что указывает на их устойчивость при средних температурах. [24]
В случае самовоспламенения летучего гидрида из-за разгерметизации аппаратуры следует прежде всего устранить возможность утечки, перекрыв отдельные участки технологической системы, а затем приступить к тушению пламени. [25]
Для элементов, образующих летучие гидриды, в частности As, Bi, Ge, Sb, Se и Те [4], существует другой способ подготовки пробы. Гидриды получают реакцией солей этих элементов с щелочным раствором борогидрида натрия. Летучие вещества затем уносятся из раствора с потоком воздуха прямо в атомизатор атомно-абсорбционного спектрофотометра. Часто используется водородно-воздушное пламя; подогреваемая снаружи кварцевая трубка-кювета позволяет спуститься до более низких концентраций вследствие увеличения времени пребывания в ней атомов. [26]
Наличие дипольного момента у летучих гидридов H2S, HBr, HC1 не вызывает деформации их кристаллической решетки. Они так же, как и благородные газы, имеют кубическую, гранецентрированную решетку. Связь в кристалле, несмотря на относительно большой диполный момент, обусловлена главным образом дисперсионными силами. Для летучих гидридов, дипольный момент которых сказывается на структуре кристаллической решетки, как, например, Н2О и NH3, Никитин не получил изоморфной смешиваемости с радоном и аргоном. [27]
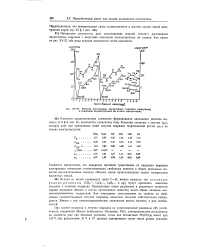 |
Энергии диссоциации двухатомных гидридов ( ккал / моль и ионизации иэоэлектронных им атомов ( ккал / г-атом. [28] |
При замене водорода в летучих гидридах на углеводородные радикалы ( R) устойчивость соединений обычно повышается. Например, РЬЩ самопроизвольно распадается на элементы уже при обычных условиях, тогда как бесцветный РЬ ( СНз) 4 кипит при ПО С без разложения. [29]
При замене водорода в летучих гидридах на углеводородные радикалы ( R) устойчивость соединений обычно повышается. Например, PbHi самопроизвольно распадается на элементы уже при обычных условиях, тогда как бесцветный РЬ ( СН3Ь кипит при 110 С без разложения. В V и VI группах одновременно имеет место резкое усиление склонности к реакциям присоединения. Иногда замена водорода на углеводородный радикал ведет даже к повышению максимальной валентности элемента. [30]
Страницы: 1 2 3 4