Высший гидрид
Cтраница 1
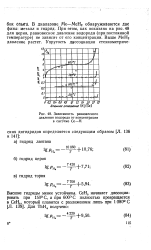 |
Зависимость равновесного. [1] |
Высшие гидриды менее устойчивы. [2]
Высшие гидриды еще менее устойчивы. [4]
Высший гидрид таллия в виде полимера ( ТЩз) белого цвета был получен аналогично соответствующему соединению индия. Он легко отщепляет водород, образуя коричневый гидрид ( TIH), устойчивый при комнатной температуре в отсутствие влаги. [5]
Высший гидрид таллия в виде полимера ( Т1Н3) Ж белого цвета получается аналогично соответствующим соединениям галлия и индия. Легко отщепляет водород - образуется коричневый гидрид ( Т1Н) Ж, устойчивый при комнатной температуре в отсутствии влаги. [6]
Высший гидрид таллия в виде полимера ( Т1Н3) Т белого цвета был получен аналогично соответствующему соединению индия. [7]
Такого рода высшие гидриды палладия, которые можно рассматривать как пергидриды, играют, повидимому, существенную роль при расщеплении воды системой гипофосфит - палладий. Вопрос этот будет более подробно изложен в одном из последующих сообщений. Здесь можно только предварительно указать на то, что, по всей вероятности, вода участвует в распаде пергидрида палладия таким образом, что промежуточно образуется чрезвычайно неустойчивая ( до сих пор гипотетическая) закись водорода или пергидрид кислорода. Если допустить, что в растительном и животном организме расщепление воды происходит посредством системы окисляемое вещество - вещество, поглощающее водород, то промежуточные пергидриды и пергидрид кислорода должны иметь для биохимических восстановительных процессов такое же значение, как перекиси и перекись водорода для биохимических окислительных процессов. На основании этих представлений, которые, конечно, можно рассматривать только как ориентирующую гипотезу, и была подвергнута мною исследованию область биохимических восстановительных процессов. [8]
При образовании высшего гидрида исходная заготовка сильно увеличивается в объеме и превращается в крупнозернистый порошок. Затем проводится полное термическое разложение обоих гидридов в вакууме при нагревании до температуры обычно выше 700J, но намного ниже 900 с целью уменьшения нежелательного спекания образующегося порошка металла. Гидриды тория вступают в реакцию с кислородом, галогенами, галогено-водородамп п водой. Оба гидрида тория пирофорны. [9]
Якель [284] установил, что высший гидрид циркония обладает кубоцентрированной тетрагональной решеткой при всех температурах; никаких изменений при 300 - 778 им не обнаружено. [10]
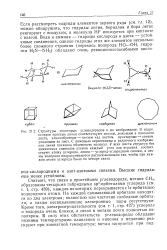
Диалогичная структура можэт быть написана для высших гидридов. Предположительно некоторый резонанс среди нескольких форм представляется менее удовлетворительным, но проблема структуры еще исследуется. [11]
Мостиковые атомы водорода между двумя группами ВН2 существуют только в В2Не и ВзНа и не найдены в высших гидридах. [12]
Известны все возможные насыщенные цепочечные гидриды Si и Ge вплоть до Si6H14 и Ge8Hi8, а также некоторые изомеры высших гидридов. Эти бесцветные соединения гораздо более реакционноспо-собны, чем углеводороды. Силильная группа SiH3 привлекает большое внимание благодаря возможности л-связи с соседями. [13]
Гидриды элементов подгруппы германия общей формулы ЭН2 не характерны. Напротив, высшие гидриды элементов ЭН4 ( кроме РЬН4) хорошо изучены. Существование гидрида свинца сомнительно. Косвенным признаком возможности образования РЬН4 ( плюмбана) является заметная летучесть свинца в токе водорода. Способность к образованию гомоатомных цепей Э - Э быстро снижается от германия к свинцу, термическая устойчивость уменьшается в этом же направлении. [14]
Гидриды элементов подгруппы германия - общей формулы ЭН2 не характерны. Напротив, высшие гидриды элементов ЭН4 ( кроме РЬН4) хорошо изучены. Существование гидрида свинца сомнительно. Косвенным признаком возможности образования РЬН4 ( плюмбана) является заметная летучесть свинца в токе водорода. Способность к образованию гомоатомных цепей Э - Э быстро снижается от германия к свинцу, термическая устойчивость уменьшается в этом же направлении. [15]
Страницы: 1 2