Высший гидрид
Cтраница 2
В настоящем Справочнике рассматриваются только простейшие гидриды серы - сероводород H2S и гидросульфил HS. Известны также высшие гидриды серы - H2S2, H2S3 H2S4 и др. Однако все эти соединения непрочные и при высоких температурах легко разлагаются. [16]
Для описания низших гидридов удобно пользоваться понятием о трехцентровой связи. Для пентаборана-9 это приближение уже менее удовлетворительно, а для высших гидридов необходимо привлекать теорию МО. [17]
Гидриды элементов V группы: фосфин, арсин и стибин являются легковоспламеняющимися веществами. Хотя чистые гидриды в смеси с воздухом не способны к самопроизвольному воспламенению, при наличии в них примесей, в частности высших гидридов, такое воспламенение может произойти. Поэтому все работы с этими гидридами следует проводить в аппаратуре, тщательно освобожденной от воздуха. Особую опасность представляют осадки высших гидридов, иногда отлагающиеся на стенках аппаратуры и в других местах при работе с фосфином. [18]
Известные гидриды кремния, или силаны, синтезируют действием минеральных кислот на силицид магния ( приблизительная формула Mg2Si), который получают восстановлением кремния металлическим магнием. Из-за аналогичной реакции - образования следов силана при взаимодействии с силицидом железа - возникает затхлый запах, часто замечаемый при выливании кислот в чугунные канализационные трубы. Остальные 5 % - высшие гидриды, главным образом пента - и гексасиланы. [19]
Была определена теплота растворения силанов в силиконовом масле и показано, что для членов гомологического ряда силанов lg VR линейно связан с числом атомов Si в молекуле кремневодородов. На этой же неподвижной фазе, нанесенной на целит, удалось разделить высшие гидриды германия [98], полученные при пропускании моногермана через тихий электрический разряд. [20]
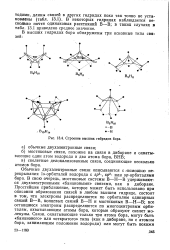 |
Строение высших гибридов бора. [21] |
Обычные двухэлектронные связи описываются с - помощью перекрывания ls - орбиталей водорода с sp3 -, sp2 - или sp - орбиталями бора. В свою очередь, мостиковые системы В - Н - В удерживаются двухэлектронными банановыми связями, как в диборане. Простейшее приближение, которое может быть использовано при описании образования связей в любом высшем гидриде, состоит в том, что электроны распределяются по орбиталям одинарных связей В-В, концевых связей В - Н и мостиковых В - Н - В; все оставшиеся электроны распределяются по многоцентровым орбиталям, охватывающим атомы бора, которые образуют скелет молекулы. [22]
Гидриды элементов V группы: фосфин, арсин и стибин являются легковоспламеняющимися веществами. Хотя чистые гидриды в смеси с воздухом не способны к самопроизвольному воспламенению, при наличии в них примесей, в частности высших гидридов, такое воспламенение может произойти. Поэтому все работы с этими гидридами следует проводить в аппаратуре, тщательно освобожденной от воздуха. Особую опасность представляют осадки высших гидридов, иногда отлагающиеся на стенках аппаратуры и в других местах при работе с фосфином. [23]
Одним из перспективных методов получения полупроводниковых элементов высокой чистоты является так называемый гидридный метод, заключающийся в термическом разложении гидрида на элемент и водород, который легко может быть удален из сферы реакции. Основное преимущество гидридного метода получения чистых элементов заключается в возможности осуществления многократной очистки элементов от примесей при получении, очистке и разложении гидрида. При получении гидрида элемент освобождается от примесей других элементов, которые не могут в условиях синтеза гидрида давать летучие соединения. При этом обычно используются простейшие гидриды элементов, так как устойчивость высших гидридов относительно невелика и получение их идет с меньшим выходом. [24]
Известны следующие гидриды: Н О, H2S, H. Свойства воды, имеющие особый характер, описаны в другой главе ( стр. Соединения серы, селена и теллура окисляются с различной быстротой; например, все они окисляются до элементов солями трехвалентного железа, a H2Se и Н Те - также солями двухвалентной ртути. В противоположность этим соединениям вода не обладает восстанавливающими свойствами. Кислород имеет только два гидрида, Н2О и Н2О2, а сера образует ряд гидридов. В высших гидридах углерода и кремния атомы этих элементов образуют цепи или кольца, используя для этого две связи на каждый атом, а две другие связи насыщаются атомами водорода. Сера, однако, обладает в гидридах только двумя связями, вследствие чего атомы водорода присоединяются только к крайним атомам серы. [25]
Страницы: 1 2