Гидрирование - ацетофенон
Cтраница 2
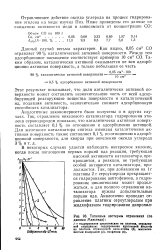 |
Типичные изотермы. [16] |
Так, при добавлении на 1 г платины 2 г сероуглерода прекращается гидрирование ацетофенона, а гидрирование циклогексана может продолжаться, и для полного отравления катализатора нужны дополнительные порции яда. [17]
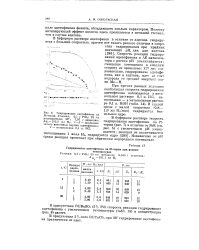 |
Гидрирование ацетофенона на Pt-черни. Условия. ОД г РЮ2. 25 мл растворителя. 30. 7 07 г вещества. Ан2202 2 мл Нг. 1 - 3 - последовательно внесенные порции ацетофенона. 4 - метанольная ОД н. НС1. [18] |
В присутствии Pd / BaS04 ( 5 % Pd) скорость реакции гидрирования ацетофенона с увеличением температуры ( табл. 15) и концентрации ( рис. 8) растет. [19]
На Pd / BaS04 ( см. табл. 15) в отличие от Pt-черни ( см. табл. 13) гидрирование ацетофенона осуществляется при большем смещении потенциала в анодную сторону. [21]
В кислой среде ярко проявляется зависимость скорости гидрирования кетона от энергии связи металл - водород: относительная скорость гидрирования ацетофенона на платине вдвое, бензофенона - в 10 раз выше, чем на палладии. [22]
По данным [272], увеличение количества уксусной кислоты в бинарном растворителе ( СН3ОН - СН3СООН) приводит к увеличению скорости гидрирования ацетофенона на Rh-В / С-катализаторе. [23]
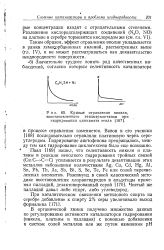 |
Кривые отравления никеля. [24] |
Вавон и его ученики [168] последовательно отравляли платиновую чернь сероуглеродом. Гидрирование ацетофенона прекращалось, между тем как гидрирование циклогексена было еще возможно. [25]
Наличие кислородного атома в - положении по отношению к бензольному ядру значительно снижает прочность соединения. Целью гидрирования ацетофенона может быть как частичное гидрирование карбонильной группы с получением ароматического спирта ( метилфенилкарбинола), так и полное гидрирование карбонильной группы и бензольного ядра. [26]
Однако оказалось, что IB тех случаях, когда хотя бы один из радикалов кетона был арилом, гидрирование проходит более глубоко и в результате образуется углеводород. Так, при гидрировании ацетофенона и бензофенона образуются этилбензол и дифенилметан соответственно. [27]
На реакцию гидрогенизации ацетофенона влияет среда, в которой осуществляется гидрирование. Как показано [179, 281], скорость гидрирования ацетофенона на NiR, промотированном платиной, с ростом рН увеличивается, при подкислении раствора уменьшается. То же наблюдается и при гидрировании бензофенона и циклогексанона. На Pt-черни, согласно [171], с ростом рН скорость гидрирования ацетофенона уменьшается. [28]
Ацетофенон, являясь простейшим жирно-ароматическим кетоном, в реакции гидрогенизации ведет себя не только как ароматический ке-тон, но и проявляет свойства, характерные для алифатических кето-нов, - способен к энолизации. В зависимости от условий проведения реакции гидрирования ацетофенона он превращается в разные продукты. Так, на Pt-черни при комнатной температуре и обычном давлении ацетофенон в зависимости от растворителя ( среды) дает различные продукты превращения: в нейтральной среде ( диоксан) образуется ме-тилфенилкарбинол, в кислой ( уксусная кислота) - этилбензол, а-цик-логексилэтанол и этилциклогексан [188], на Pt-черни ( по Адамсу) в спиртовом растворе НС1 - этилциклогексан. [29]
Одним из наиболее перспективных методов получения ВЦГ является его синтез из ацетофенона [134, 135], представляющего собой побочный продукт производства фенола и ацетона кумольным способом. Процесс получения ВЦГ включает две стадии: гидрирование ацетофенона в метил-циклогексилкарбинол и дегидратацию метилциклогексилкарбинола с образованием ВЦГ. Оптимальным катализатором гидрирования ацетофенона по селективности и выходу целевого продукта ( 90 - 95 %) является родий на оксиде алюминия. [30]
Страницы: 1 2 3