Гидрирование - нитрил
Cтраница 3
Гидрирование соединений с открытыми цепями, которые содержат азот в ненасыщенной форме, в том числе гидрирование нитрилов, нитрозо - и диазосоединений рекомендуется проводить, добавляя кроме катализатора также электролит ( например раствор KCN, FeSO4, NiSO4), который может отщепить эквивалентное образовавшемуся основанию количество кислоты тза. [31]
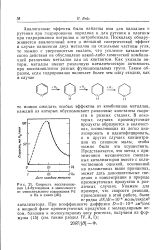 |
Скорость восстановле - - . [32] |
Аналогичные эффекты были найдены ими для палладия п рутения при гидрировании пиридина и для рутения и платины при гидрировании нитрилов и нитробензола. Поскольку обнаруживается аналогичный хотя и меньший синергический эффект в случае нанесения двух металлов на отдельные частицы угля, то можно с уверенностью сказать, что усиление каталитического действия не обусловлено какой-либо химической комбинацией различных металлов или их контактом. Как указали авторы, металлы имеют различную каталитическую активность при восстановлении разных функциональных групп. [33]
Во втором случае реакции разделяют: на первой стадии проводят дегидратацию ( путем аммонолиза) жирных кислот с образованием нитрилов, на второй стадии проводят гидрирование нитрилов с образованием первичных алкиламинов. [34]
При гидрировании циануксусной кислоты [111] или ее соли [1 12 ] в спиртовом растворе со скелетным никелевым катализатором реакция образования Р - аланина при 90 С проходит за 15 мин, прибавление аммиака способствует более полному гидрированию нитрильной группы в первичную аминогруппу за счет снижения количества вторичных аминов, всегда образующихся при каталическом гидрировании нитрилов. [35]
Нитрилы, азометины, оксимы и др. легко восстанавливаются над платиной или палладием, в то время как для восстановления над скелетным никелем требуется температура - 100 С. При гидрировании нитрилов в качестве побочных продуктов образуются очень часто вторичные и третичные амины. [36]
Тройная связь CN нитрилов может вступать во многие реакции присоединения, некоторые из которых широко применяются в синтезах. Напомним здесь гидрирование нитрилов натрием в спирте, литийалюми-нийгидридом или каталитическим путем, приводящее к получению первичных аминов, и присоединение магнийорганических соединений, в результате которого образуются кетимины и затем кетоны. Мягким восстановлением ароматических нитрилов хлористым оловом в сухом эфире получаются ароматические альдегиды. [37]
Преимущественное образование вторичных аминов объясняется склонностью первичных аминов к конденсации с альдиминами. Направление реакции гидрирования нитрилов зависит от катализатора и условий. Применение Ni Ренея способствует преимущественному образованию первичных аминов. [38]
Реакция, как правило, сопровождается образованием аминов более высокой, чем заданная, степени алкилирования, так как первичный амин, получающийся при восстановительном алкилиро-вании аммиака, частично реагирует с карбонильным соединением и дает вторичный амин, который, в свою очередь, может тем же путем превращаться в третичный амин. Кроме того, как и при гидрировании нитрилов, возможны процессы конденсации с участием ин-термедиатов ( см. 1.6.5), увеличивающие, особенно при повышенных температурах, выход тех же побочных продуктов. Преимущественное получение амина заданной степени алкилирования определяется соотношением реагентов. Его доля в продуктах алкилирования заметно зависит также от строения карбонильного соединения и условий реакции. [39]
Гораздо меньше исследована реакция получения аминометилпи-ридинов при каталитическом гидрировании моноцианпиридинов. Известно лишь, что названные амины образуются при гидрировании нитрилов при повышенных [12, 13] или высоких [14] давлениях водорода на никелевых катализаторах в присутствии концентрированного аммиака. Между тем аминометилпиридины являются ценными мономерами для производства полимерных материалов и ионообменных смол. [40]
Метод получения нитрилов и аминов на основе жирных кислот был впервые разработан фирмой Armour ( США) и реализован в 1942 г. на одном из ее заводов. Процесс включает две стадии: аммонолиз жирных кислот в нитрилы и гидрирование нитрилов в соответствующие амины. Первая стадия осуществляется на проточной установке непрерывного действия, вторая - в периодически действующих автоклавах. [41]
Никаких сведений по технологии процесса фирма не публикует, кроме принципиальной технологической схемы. На основании этой схемы можно сделать вывод о том, что гидрирование нитрилов осуществляется в растворителе с применением суспензированных катализаторов. [42]
Предполагается, что промежуточными продуктами здесь являются азометины и енамины. И в этом случае необходимо считаться с возможностью побочных реакций, упомянутых при рассмотрении гидрирования нитрилов. [43]
В то же время по своей реакционной способности нитрилы фторуглеродов лишь незначительно отличаются от органических нитрилов. Нитрилы фторуглеродов при температуре около 50 легко гидролизуются водной щелочью с образованием кислой соли и аммиака, причем атом фтора остается в молекуле. В результате гидрирования нитрилов над окисью платины, применяемой в качестве катализатора, с хорошим выходом получаются амины. Эта реакция, однако, очень чувствительна к изменениям условий. В качестве промежуточного продукта этой реакции образуется фторсодержа-щий найлон, представляющий большой интерес. [44]
В последнее время усиленно развивается новое на-правление, для которого характерны различные формы использования ионитов как сокатализаторов и носителей других катализаторов. В работе25 катионит амберлист-15 используется совместно с никелем Ренея, благодаря чему удается совместить реакции гидрирования нитрилов и гидролиза образующихся иминов. При этом катионит выступает не только как катализатор, но и в своей ионнообмен-ной функции, поглощая аммиак, выделяющийся при гидролизе имива. [45]
Страницы: 1 2 3 4