Гидрирование - последнее
Cтраница 2
Авторы считают, что первым актом реакции является стадия алкилирования комплекса переходного металла бутиллитием, в результате чего образуется а-связан-ное металлоорганическое соединение. Гидрирование последнего приводит к образованию гидрида металла, который при взаимодействии с олефином дает я-комплекс. Дальнейшее превращение этого я-комплекса в сг-комплекс и гидрогенолиз последнего водородом приводит к регенерации гидрида переходного металла и образованию продукта реакции. По мнению авторов, гидрирующая способность катализатора зависит главным образом от природы центрального элемента я-комплекса. [16]
Таким образом, конденсация кетоспиртов и кетоэфиров с простыми эфи-рами третичных ацетиленовых карбинолов в условиях реакции Фаворского протекает гладко, с образованием моно - и диэфиров ацетиленовых глицеринов. Гидрирование последних на платиновом и палладиевом катализаторах приводит к моно - и дизфирам глицеринов этиленового ряда, а ал-жилирование и ацетилирование приводит к полным простым и смешанным зфирам а цетиленового ряда. [17]
Применение, о-хинондиазидов, содержащих конденсированные бензольные ядра, позволяет перейти от простейших производных индена к более сложным. При гидрировании последнего получается циклопентенфенантрен, соединение, обнаруженное среди продуктов распада холестерина. [18]
В полном синтезе хинина ( Р. Б. Вудворд и В. Е. Деринг, 1944 г.) исходят из 7-оксиизохинолина, полученного при конденсации л - оксибензальдегида с ацеталем аминоацетальдегида и циклизации под действием серной кислоты. Каталитическое гидрирование и последующее ацетилирование приводят к получению соединения IV; в результате гидрирования последнего получается смесь двух стереоизомерных кето-нов V и VI, из которой цмс-изомер V был выделен в виде кристаллического гидрата. [19]
Этим методом получают большие количества к-бутанола. Сущность метода заключается в альдолизации ацетальдегида, дегидратации ацетальдоля в кро-тоновый альдегид и гидрировании последнего до н-бутанола. [20]
Получают взаимодействием а со-диолов с а ю-дигалоге-нидами или а ю-дитозилатами в присутствии оснований. Наиболее часто используются 18-краун - 6 ( ф-ла И), сши-дибензо-18 - краун-б и продукт гидрирования последнего - дициклогексилен-18 - краун-6. Применяются для разделения катионов в аналитической химии и получения р-ров солей в органических ц р-рителях. [21]
Скорости гидрирования алкенов и алкадиенов и их производных различны. При гидрировании бензинов, содержащих различные по химическому характеру непредельные соединения, большая часть их гидрируется очень быстро; гидрирование последних оставшихся еще не прогидрированными непредельных соединений протекает медленно и требует затраты значительного количества времени. [22]
На первом этапе было исследовано гидрирование некоторых моделирующих азотистых соединений в присутствии промышленного кобальтмолибденового катализатора. В большинстве опытов применяли хинолин, в котором помимо содержащего азот кольца в нем имеется ароматическое кольцо, что давало возможность установить интенсивность нежелательного гидрирования последнего. [23]
Видно, что изомеризация олефинов затрагивает больше 90 % сырья, причем с понижением температуры равновесный выход изомеров возрастает. По-скольку, однако, в продуктах гидрокрекинга содержатся не изоолефины, а изопарафины, необходимо оценить термодинамическую вероятность превращения изоолефинов в изопарафины за счет гидрирования последних. [24]
При взаимодействии эквимолярных количеств ацетилена и формальдегида образуется пропаргиловый спирт ( 12), который окисляется в присутствии хлорной меди в гексадиин-2 4-диол - 1 6 ( 13); гидрированием последнего получают гександиол-1 6 ( 14), превращающийся при окислении в адипиновую кислоту. [25]
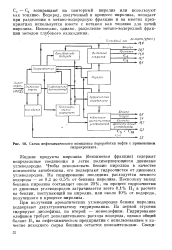 |
Схема нефтехимического комплекса переработки нефти с применением. [26] |
Жидкие продукты пиролиза ( бензиновая фракция) содержат непредельные соединения и легко полимеризующиеся диеновые углеводороды. Чтобы использовать бензин пиролиза в качестве компонента автобензина, его подвергают гидроочистке от диеновых углеводородов. На гидрирование последних расходуется немного водорода - от 0 2 до 0 5 % от бензина пиролиза. Поскольку выход бензина пиролиза составляет около 20 %, на процесс гидроочистки от диеновых углеводородов затрачивается всего 0 1 % Н2 в расчете на бензин, поступающий на пиролиз, или около 10 % от водорода, полученного в процессе пиролиза. [27]
Применение о-хинондиазидов, содержащих конденсированные бензольные ядра, позволяет перейти от простейших производных индена к более сложным. При гидрировании последнего получается циклопентенфенантрен, соединение, обнаруженное среди продуктов распада холестерина. [28]
Селективное гидрирование, осуществляемое на палладиевых или медь-никелевых катализаторах с введением близкого к сте-хиометрическому количества водорода, позволяет провести процесс превращения ацетилена в этилен. В промышленных условиях реализован также процесс очистки циклогексана от бензола гидрированием последнего на никелевых катализаторах. Гидрирование примесей олефинов и ароматических углеводородов является этапом получения чистых парафинов. [29]
Сырьем для производства D-сорбита в настоящее время служит D-глюко-за, кторая является сравнительно дорогим видом сырья. Барышева [60, 61 ] разработали метод получения D-сорбита из непищевого растительного сырья ( хлопковый линт, сульфитная целлюлоза) путем гидролитического гидрирования последних. Процесс представляет собой совмещение двух каталитических реакций - гидролиза полисахаридов с образованием моноз и гидрирования последних в многоатомные спирты. Этот метод является весьма перспективным, но в связи с дороговизной катализаторов требует тщательной технологической отработки. [30]
Страницы: 1 2 3