Гидрирование - бензольное ядро
Cтраница 1
Гидрирование бензольного ядра было впервые испробовано с помощью иодистоводородной кислоты. При нагревании бензола с большим избытком очень концентрированной иодистоводородной кислоту образуется углеводород Бертло 891, который считался нормальны гексаном. [1]
Гидрирование бензольного ядра в бензальдегиде, бензофеноне и других соединениях удается провести посредством водорода и коллоидной платины, если подходящим образом защитить СНО - или СО-группы. [2]
Реакция гидрирования бензольного ядра в ароматических кислотах происходит гораздо легче, чем в ароматических углеводородах. [3]
Скелетный никель как катализатор гидрирования бензольных ядер по своей эффективности уступает, по-видимому, никелю на кизельгуре. Даже с большим количеством первого катализатора и при более высоких температурах восстановление протекает медленнее. [4]
Второе бензольное ядро после гидрирования не изменяет скорости гидрирования оставшегося бензольного ядра, например в бифениле из. [5]
Для углеводородов, содержащих ароматические кольца, характерны реакции деалкилирования и гидрирования бензольного ядра. Образующиеся при этом нафтеновые углеводороды вступают в реакции, описанные выше. Для гибридных молекул типа тетралина возможно, наоборот, накопление бензола в результате раскрытия нафтенового кольца и дальнейшего гидродеалкилирования. Конденсация полициклических систем под давлением водорода полностью тормозится. [6]
Для углеводородов, содержащих ароматические кольца, характерны реакции деалкилирования и гидрирования бензольного ядра. Образующиеся при этом циклоалканы вступают в реакции, описанные выше. Для гибридных молекул типа тетралина возможно, наоборот, накопление бензола в результате раскрытия циклоалканового кольца и дальнейшего гидродеалкилирования. Конденсация полициклических систем под давлением водорода полностью тормозится. Реакция гидрирования бензольного кольца при температурах выше 300 С характеризуется положительным значением AG. Поэтому для сдвига равновесия в сторону образования насыщенных колец необходимо повышенное давление водорода. Именно эти условия и характерны для гидрокрекинга. [7]
Для углеводородов, содержащих ароматические кольца, характерны реакции деалкилирования и гидрирования бензольного ядра. Образующиеся при этом нафтеновые углеводороды вступают в реакции, описанные выше. Для гибридных молекул типа тетралина возможно, наоборот, накопление бензола в результате раскрытия нафтенового кольца и дальнейшего гидродеалкилирования. Конденсация полициклических систем под давлением водорода полностью тормозится. Реакция гидрирования бензольного кольца при температурах выше 300 С характеризуется положительным значением AG. Поэтому для сдвига равновесия в сторону образования насыщенных колец необходимо повышенное давление водорода. Именно эти условия и характерны для гидрокрекинга. [8]
Для углеводородов, содержащих ароматические кольца, характерны реакции деалкилирования и гидрирования бензольного ядра. Образующиеся при этом циклоалканы вступают в реакции, описанные выше. Для гибридных молекул типа тетралина возможно, наоборот, накопление бензола в результате раскрытия циклоалканового кольца и дальнейшего гидродеал-килирования. Конденсация полициклических систем под давлением водорода полностью тормозится. Реакция гидрирования бензольного кольца при температурах выше 300 С характеризуется положительным значением AG. Поэтому для сдвига равновесия в сторону образования насыщенных колец необходимо повышенное давление водорода. Именно эти условия и характерны для гидрокрекинга. [9]
В этих случаях, используя разницу в температурах, необходимых для гидрирования бензольного ядра и боковой цепи ( гидрирование которой, как правило, происходит легче гидрирования ядра), удается проводить избирательную гидрогенизацию боковой цепи, не затрагивая бензольного кольца. Значительно активнее, по некоторым данным, катализатор Бага, который количественно восстанавливает фенол в циклогексанол при 2 - 3 am и 60, а нафталин при 200 -в тетралин. Интересно также отметить, что легкость гидрирования бензольного кольца, входящего в сложном соединении в боковую цепь, в значительной степени зависит от того, каким образом присоединяется это кольцо. [10]
Поскольку соединение D отличается от соединения С только двумя атомами водорода, значит гидрирование бензольного кольца в соединении С не произошло ( при гидрировании бензольного ядра присоединяются три молекулы Й2 и водород присоединился по карбонильной группе. [11]
На потенциальной кривой, полученной, например, при гидрировании фенилацетилена в спирте, ясно можно видеть переломы при переходах от гидрирования тройной связи к гидрированию двойной ( стирол) и затем к гидрированию бензольного ядра. [12]
Основным превращением н-бутилбензола в принятых условиях является частичный и полный гидрогенолиз боковой цепи с образованием н-пропилбензола, этилбензола, толуола и бензола. Кроме того, наблюдаются также реакции гидрирования бензольного ядра, сжатия гексаметиленового цикла в пятичлен-ный, гидрогенолиз последнего, образование ксилолов, метилпро-пилбензолов, диэтилбензолов и дегидроциклизация боковой цепи н-бутилбензола с образованием нафталина. [13]
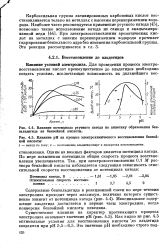 |
Влияние потенциала ртутного йатода на кинетику образования бен-зальдегида из бензойной кислоты.| Влияние рН на процесс электрохимического восстановления бензойной кислоты. [14] |
Карбоксильная группа активированных карбоновых кислот восстанавливается только на металлах с высоким перенапряжением водорода. При электровосстановлении ароматических кислот на металлах с низким перенапряжением водорода протекает гидрирование бензольного ядра без изменения карбоксильной группы. Эта реакция рассматривается в гл. [15]
Страницы: 1 2