Гидро-пероксид
Cтраница 2
Так, предлагалось окислять циклоалканы С8 и Ci2 до гидро-пероксидов с разложением последних щелочью до смеси спирта с кетоном. Эти условия, аналогично окислению парафинов, способствуют преимущественному образованию спирта по сравнению с кетоном. [16]
 |
Технологическая схема окисления циклогексана в смесь анола и анона. [17] |
Так, предлагалось окислять циклоалканы Се и Ci2 до гидро-пероксидов с разложением последних щелочью до смеси спирта с кетоном. Эти условия, как показано ранее ( стр. [18]
Добавление в раствор соединений, способных к образованию с гидро-пероксидом прочных ассоциатов, разрушает гомоассоциаты гидропероксидов. Это приводит к мономолекулярному по гидропероксиду распаду. [19]
Оксидат из нижней части колонны / содержит до 30 % гидро-пероксида. Он отдает свое тепло изопропилбензолу в теплообменнике 4, дросселируется до остаточного давления ж 4 кПа и поступает на вакуум-ректификацию для концентрирования гидроперок-сида. Отгонку изопропилбензола ведут в насадочной ректификаци-снной колонне 6 непрерывного действия, снабженной конденсатором-дефлегматором. Применение вакуума обусловлено термической нестабильностью гидропероксида. Часть конденсированного изопропилбензола возвращают из конденсатора-дефлегматора на орошение колонны 6, а остальное количество выводят в сепаратор 3, громывают щелочью и снова направляют на окисление. Кубовая жидкость из колонны 6 содержит 70 - 75 % гидропероксида, а также побочные продукты окисления и остатки изопропилбензола. Следующую стадию ( кислотное разложение гидропероксида) осуществляют в узле 7 одним из двух списанных выше методов. [20]
Также были найдены константы скоростей реакций термического, термокатапитического и индуцированного распада гидро-пероксидов ацеталей. Было установлено, что соединения DOjH в интервале температур 60 - S-120 С с выходами, близкими к количественному образуют соответствующие моноэфи-ры гликолей. [21]
Анализ данных табл. 1 показывает, что прочность двойных комплексов катализатора с гидро-пероксидом и олефином уменьшается, а тройной комплекс становится прочнее. Из табл. 2 видно, что увеличение температуры способствует повышению скорости реакции эпоксидирования моноокиси больше, чем диена. Это можно объяснить специфичностью координации моноокиси, которая в этой реакции является одновременно и субстратом и ингибитором. [22]
Поскольку подобные соединения можно рассматривать как кислые соли пероксида водорода, их часто именуют гидро-пероксидами. Характерное свойство пероксидов металлов, пероксокислот и гид-ропероксидов - способность подвергаться гидролизу с образованием пероксида водорода и разлагаться, выделяя кислород, т.е. быть окислителями. [23]
Препаративное разделение в условиях работы [ Ю ] обеспечивает получение 10 - 1ОО мг образцов гидро-пероксидов из полиненасыщенных кислот или их эфиров за одну операцию. [24]
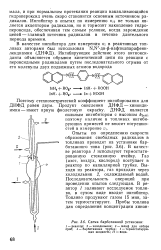 |
Схема барботажной установки. [25] |
Ингибитор в опытах по измерению и-о не только является акцептором радикалов, но и тормозит накопление гидро-пероксида, обеспечивая тем самым условие, когда зарождение цепей - главный источник радикалов в течение длительного периода времени. [26]
При фотоокислении ПСХ-ЛС протекают одновременно два процесса: дегидрохлорирование по радикально-цепному механизму и окисление с образованием гидро-пероксидов и карбонильных групп. Продукты окисления в результате фотолиза за счет собственного поглощения в ближней ультрафиолетовой области спектра в свою, очередь генерируют свободные радикалы, которые инициируют дегидрохлорирование и образование двойных связей. [27]
Для производства другого ценного продукта - фенола - используют кумол ( изопропилбензол), который окисляют в гидро-пероксид, разложением которого кислотой получают фенол. [28]
Пероксидные соединения, главным образом пероксид водорода и надуксусная кислота ( а в последнее время - и гидро-пероксиды), получили применение как окислительные агенты в основном органическом и нефтехимическом синтезе сравнительно недавно. Ввиду относительной дороговизны их используют только для таких реакций, которые не протекают под влиянием молекулярного кислорода или азотной кислоты. [29]
В другой работе ( Романцев и Левин) было показано, что на ртутном капающем электроде восстанавливаются все гидро-пероксиды и низшие диалкилпероксиды, в то время как из-за пространственных затруднений более сложные пероксиды не поддаются восстановлению. [30]
Страницы: 1 2 3 4