Гидрогенолиз - соединение
Cтраница 2
Был поставлен опыт по избирательному каталитическому гидрированию многокомпонентной смеси сераорганических соединений с целью проверки, насколько надежно будет сохраняться избирательность гидрогенолиза соединений различного строения в такой сложной смеси. ГидрЪгенизат этой смеси содержал 0 11 % серы, что точно соответствовало количеству ее, содержавшемуся в навеске дибензтиофена, внесенного в исходную смесь. [16]
Главное преимущество этого метода по сравнению с другими методами определения галогенов, основанными на реакции восстановления, состоит в его простоте, поскольку он позволяет осуществлять гидрогенолиз галогенор-ганических соединений в стакане без применения заранее приготовленного катализатора, специальной аппаратуры для гидрирования и газгольдера с водородом. Данные, приведенные в табл. 8, иллюстрируют точность и чувствительность метода. [17]
 |
Молярные радиоактивности ненасыщенных соединений ( введение метки изотопным обменом на гетерогенных катализаторах платиновой группы. [18] |
Кроме влияния на химический выход и распределение метки в молекулах органических соединений, природа активированного трития может определять даже саму возможность получения меченых аналогов некоторых лабильных в условиях гидрогенолиза соединений. [19]
Параллельно образуются шпинельные фазы типа алюминатов кобальта ( никеля) и молибдата алюминия, в которых гидрирующие металлы связаны прочно, не сульфидируются и не принимают участия в гидрогенолизе соединений серы и азота. При увеличении общего содержания Ni ( Co) Mo в составе катализатора, синтезируемого методом соэкструзии, происходит насыщение носителя ( М20з) металлами, входящими в состав шпинельных фаз, и растет относительное содержание никель ( кобальт) молибдатов и алюмоникель ( кобальт) молибда-тов. [20]
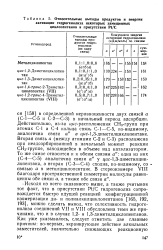 |
Относительные выходы продуктов и энергии. [21] |
Исходя из всего сказанного выше, а также учитывая тот факт, что в присутствии Pt / C гидрогенолиз сопровождается быстро идущей реакцией конфигурационной изомеризации ди - и полиалкилциклопентанов [165, 192, 193], можно сделать вывод, что селективность гидрогенолиза соединений VII и VIII обусловлена теми же причинами, что и в случае 1 2 - и 1 3-диметилциклопентанов. [22]
Таким образом, при проведении циклооктана над никелем, отложенным на кизельгуре, в сильном токе водорода в сравнительно мягких температурных условиях ( 200 - 250 С) протекают три процесса: впервые обнаруженный нами гидрогенолиз восьмичленного цикла с образованием w - октана, аналогичный гидрогенолизу соединений с меньшими циклами [2-5], трансаннулярная дегидрогенизация, приводящая к iic - пентала-ну, и постадийная изомеризация циклооктана в соединения с семи -, шести - и пятичленными кольцами. В количественном соотношении этих процессов немаловажную роль играет температура реакции. Так, гидрогенолиз циклооктана в заметной степени протекает лишь при 200 С, а при 250 С этот процесс практически не наблюдается, тогда как образование ненталана характерно главным образом для 250 С. Процессы изомеризации циклов, сопровождаемые гидрокрекингом, идут и при 200, и при 250 С, однако при 250 С они, кроме того, осложняются еще ароматизацией гексаметиленовых углеводородов. Интересно отметить, что обнаруженный в катализатах ис-1 2-диметилциклопентан образуется, вероятно, в результате указанных процессов изомеризации. Подтверждением этому является тот факт, что в катализате, полученном при 200 С, этого углеводорода содержится больше, чем в катализате, полученном при 250 С, тогда как в случае образования мс-1 2-диметилциклопеитаиа из умс-пенталана, в результате гидрогенолиза г ис-пенталана и гидрокрекинга образующегося при этом 1-метил - 2-этилциклопентана, г / мс-1 2-диметил-циклопентана должно было бы быть больше при 250 С, так как при 200 С tyuc - пенталан почти не образуется, а 1-метил - 2-этилциклопентан в катализате вообще не найден. Уменьшение количества г с-1 2-диметилцикло-пентана при проведении реакции при 250 С можно объяснить тем, что в этом случае идут конкурирующие процессы образования из метилцикло-гексана 1 / ис-1 2-диметилциклопентана, с одной стороны, и ароматических углеводородов ( бензола и толуола), с другой, и равновесие сдвигается в сторону образования последних. При 200 С процессы ароматизации не происходят, и поэтому при этой температуре процент превращения метилциклогексана в мс-1 2-диметилциклопентан больше, чем при 250 С. [23]
Следует отметить легкость разрыва С - S-связи в ароматических сульфидах. Чтобы произошел гидрогенолиз соединения, достаточно простого кипячения его со спиртовой взвесью скелетного никеля в колбе с обратным холодильником, причем реакция протекает в настолько мягких условиях, что не происходит гидрирования ароматического кольца. [24]
Если для этого ряда принять время, при котором гидрогенолиз дифетшлсульфида происходит на 50 6, за единицу, то получим следующие относительные значения времени гидрогенолиза на 50 % остальных соединений. Эти величины ( табл. 96) характеризуют относительные скорости гидрогенолиза соединений. [25]
Основной побочной реакцией, которая в условиях проведения обессеривания всегда имеет мест, следует считать коксообразование, являющееся главным тормозящим фактором при обессеривании. Поэтому обессери-вание необходимо проводить в той оптимальной области рабочих условий, в которой гидрогенолиз сераорганиче-ских соединений идет достаточно хорошо, а реакции кок-сообразования еще не очень интенсивны. [26]
Очень кислотные точки являются достаточно сильными акцепторами электронов для того, чтобы взаимодействовать с олефинами и гидрировать их. Сероводород и серусодержащие соединения прочно адсорбируются на этих точках, также обладающих некоторой активностью для гидрогенолиза соединений серы. Слабокислотные точки, которые играют главную роль в реакции гидрогенолиза, отравляются такими сильными основаниями, как, например, аммиак. [27]
В процессе использования катализатор находится в среде водорода, сероводорода и углеводородов в паровой и жидкой фазах. Исследования показывают, что активные компоненты катализаторов в сульфидной форме, образование которой неизбежно в данной среде, характеризуются даже большей активностью в реакциях гидрогенолиза серусодержа-щих соединений. [28]
Страницы: 1 2