Гидроксид
Cтраница 3
 |
Константы ионизации К некоторых соединений и ионов в воде при 25 С. [31] |
Гидроксиды многих металлов в водных растворах могут диссо - циировать и по кислотному, и по основному типам. [32]
 |
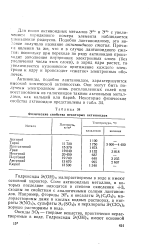
Некоторые свойства тория, урана и плутония. [33] |
Гидроксид уранила UOa ( OH) 2 амфотерен. Реагируя с кислотами, он образует соли уранила. [34]
 |
Физические свойства некоторых актиноидов. [35] |
Гидроксиды Э ( ОН) 3 малорастворимы в воде и имеют основной характер. Соли актиноидных металлов, в которых последние находятся в степени окисления 3, сходны по свойствам с аналогичными солями лантаноидов. Например, фториды ЭР3 и оксалаты Э2 ( С2О4) з малорастворимы даже в кислых водных растворах, а нитраты Э ( МО3) з, сульфаты Э2 ( 5О4) з и перхлораты Э ( С1О4) з хорошо растворимы в воде. [36]
Гидроксиды выделяются преимущественно на частицах примесей, что также способствует укрупнению частиц. [37]
Гидроксиды некоторых - элементов представляют собой слабые малорастворимые в воде основания; другие либо проявляют амфотерные свойства, либо являются определенно выраженными кислотами. [38]
Гидроксиды - аморфные осадки, труднорастворимые в воде. Обладают основным характером и, растворяясь в кислотах, образуют соли. Различная растворимость двойных сульфатов используется для разделения лантаноидов. [39]
 |
Некоторые свойства d - металлов III группы. [40] |
Гидроксиды получаются гидратацией оксидов при значительном выделении тепла. [41]
Гидроксиды Со2 1 и Со3 в зависимости от образования аквакомплек-сов и количества гидратирующих молекул воды изменяют свою окраску с розовой на синюю. Гидроксиды Ni2 и Ni3 обладают различной устойчивостью и это широко используется в технике ( стр. [42]
Гидроксиды или гидратированные оксиды всех металлов и полуметаллов, за исключением щелочных металлов, мышьяка и части щелочноземельных металлов, малорастворимы в воде, но растворимости весьма различны. [43]
Гидроксиды хорошо растворяются в воде, при этом выделяется тепло и образуются растворы, являющиеся сильными электролитами. Растворимость гидроксида лития значительно меньше, чем гид-роксидов его аналогов. [44]
Гидроксиды ( основания) - это сложные вещества, молекулы которых состоят из атома металла и одной или нескольких еидро-ксильных групп. [45]
Страницы: 1 2 3 4