Гидроксид - кобальт
Cтраница 2
Чем отличается взаимодействие гидроксидов кобальта ( III) и никеля ( III) с кислотами от взаимодействия гидроксида железа ( III) с кислотами. [16]
Испытать, растворяется ли гидроксид кобальта ( II) в разбавленных кислотах и в избытке концентрированного раствора щелочи. [17]
В отсутствие аммонийных солей гидроксид кобальта ( II) осаждается также и водным раствором аммиака. [18]
Практически нерастворимый в воде гидроксид кобальта ( Ш) Со ( ОН) 3 окрашен в темно-коричневый цвет. [19]
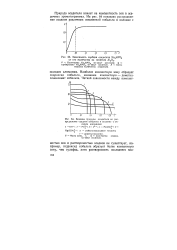 |
Зависимость сорбции осадителя Na от его количества на носителе А1203.| Влияние природы осадителя на распределение осадков кобальта в колонке с оксидом алюминия. [20] |
Наиболее компактную зону образует гидроксид кобальта, наименее компактную - диметил-глиоксимат кобальта. [21]
По свойствам он подобен гидроксиду кобальта ( III), но обладает еще более выраженными окислительными Свойствами. [22]
По свойствам он подобен гидроксиду кобальта ( III), но обладает еще более выраженными окислительными свойствами. [23]
В отдельной микропробирке вновь подучите осадок гидроксида кобальта и прилейте 3 - 4 капли концентрированного раствора едкого натра. [24]
Оксиду кобальта ( III) СоаО3 соответствует гидроксид кобальта ( III) Со ( ОН) 3 темно-коричневого цвета. Обычные соли кобальта ( III) нестойки, но комплексные соединения прочны. [25]
Оксиду кобальта ( III) Со2О3 соответствует гидроксид кобальта ( III) Со ( ОН) 3 темно-коричневого цвета. Обычные соли кобальта ( III) нестойки, но комплексные соединения прочны. [26]
Как можно показать, что оксиды и гидроксиды кобальта ( II) и никеля ( II) имеют только основной характер, Одинакова ли устойчивость степени окисления 2 для Fe, Со и Ni. Покажите это на примере свойств их гидрокси-дов. [27]
При добавлении гидроксида натрия NaOH в осадок выпадает голубой гидроксид кобальта ( II); если нагреть пробирку, он перейдет в устойчивую форму с розовой окраской. [28]
При добавлении гидроксида натрия NaOH в осадок выпадает голубой гидроксид кобальта ( II); если нагреть пробирку, он перейдет в устойчивую форму с розовой окраской. Простые соли трехвалентного кобальта в основном нестойки в растворе. [29]
 |
Спектр поглощения. [30] |
Страницы: 1 2 3 4