Гидроксид - марганец
Cтраница 3
Уменьшение концентрации маскирующего реагента определяется возможностью полного маскирования ионов Cd и образованием сопряженного осадка гидроксида марганца. [31]
Написать уравнения реакций, в которых из сульфата марганца ( II) получаются: а) гидроксид марганца ( III); б) диоксид марганца; в) марганцовая кислота. [32]
При этом на катоде выделяется осадок, содержащий только 60 - 70 % металла, остальное составляет гидроксид марганца. Для предотвращения образования гидроксида марганца в электролит вводят соли аммония. [33]
При этом на катоде выделяется осадок, содержащий только 60 - 70 % металла, остальное составляет гидроксид марганца. Для предотвращения образования гидроксида марганца в электролит вводят соли аммония. [34]
При действии щелочей на растворы солей марганца ( II) выпадает, в виде белого осадка, гидроксид марганца ( II) Мп ( ОН) 2, обладающий основными свойствами. [35]
Растворы хлорида марганца получают растворением в соляной кислоте марганцевой руды, диоксида или монооксида марганца, карбоната, гидроксида марганца и других марганецсодержащих соединений. [36]
Классическим методом определения растворенного в воде кислорода считается метод Винклера [52], основанный на реакции между кислородом и гидроксидом марганца ( И) в виде суспензии в сильнощелочном растворе. При подкислении в присутствии иоди-да окисленный гидроксид марганца снова восстанавливается до Мп11, а выделяющийся иод, количество которого эквивалентно содержанию растворенного кислорода, определяют титрованием стандартным раствором тиосульфата. [37]
Необходимо избегать изменения концентрации кислорода в пробе в периЬ я с момента ее отбора до момента фиксации, изменения состава осадка гидроксида марганца ( II) с момента его образования до начала титрования. [38]
Основным источником ошибок в определении кислорода методом Винклера является наличие в растворе окислителей, помимо кислорода, способных окислять Мп2, или восстановителей, реагирующих с гидроксидами марганца ( III) или марганца ( IV) или иодом в подкисленном растворе. [39]
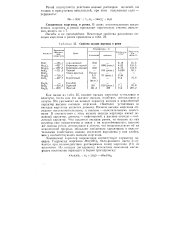 |
Свойства оксидов марганца и рения. [40] |
Химический характер гидроксидов соответствует характеру оксидов. Гидроксид марганца Мп ( ОН) 2 бело-розового цвета получается при взаимодействии растворимых солей марганца ( II) со щелочами. [41]
В основе метода лежит реакция окисления марганца ( II) в щелочной среде растворенным кислородом. Образующийся осадок гидроксида марганца ( IV) бурого цвета при последующем подкислении в присутствии иодида калия растворяется с образованием свободного иода, который определяют титрованием тиосульфатом натрия. [42]
При этом на катоде выделяется осадок, содержащий только 60 - 70 % металла, остальное составляет гидроксид марганца. Для предотвращения образования гидроксида марганца в электролит вводят соли аммония. [43]
При этом на катоде выделяется осадок, содержащий только 60 - 70 % металла, остальное составляет гидроксид марганца. Для предотвращения образования гидроксида марганца в электролит вводят соли аммония. [44]
Магний реагирует с водой только под воздействием тепла. В результате этой реакции образуются гидроксид марганца и водород. [45]
Страницы: 1 2 3 4