Гидроксил-анион
Cтраница 2
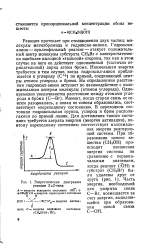 |
Энергетическая диаграмма реакции 5я2 - типа. [16] |
Реакция протекает при столкновении двух частиц: молекулы метилбромида и гидроксил-аниона. Гидроксил-анион - нуклеофильный реагент - атакует положительный центр молекулы субстрата СНзВг с электростатически наиболее выгодной тыльной стороны, так как в этом случае на него не действует одноименный ( частично отрицательный) заряд атома брома. Наименьшая энергия требуется в том случае, когда гидроксил-акион приближается к углероду ( С 6) по прямой, соединяющей центры атомов углерода и брома. Момент, когда старая связь не совсем разорвалась, а новая не совсем образовалась, соответствует ( переходному состоянию. В переходном состоянии гидроксильная группа, углерод и бром располагаются по прямой линии. Для достижения такого состояния требуется затрата энергии ( энергия активации), поэтому переходному состоянию соответствует максимальная энергия реагирующей системы. [17]
Этот механизм аналогичен рассмотренному ранее для кислотного гидролиза ДНК ( см. стр. Роль гидроксил-анионов ( как и протонов при р-элиминации, катализируемой кислотами) заключается в енолизации карбонильной группы при С-1 в открытой форме остатка дезоксирибозы, приводящей к р-элиминации З - фосфат-ной группы. Отщепление 5 -фосфатной группы может происходить либо по механизму, подобному р-элиминации, либо по механизму а-элиминации ( см. также стр. [18]
Анион Y, обычно обладает не только нуклеофильными, но и основными свойствами и может отщепить водород от ( 5-углеродного атома карбокатиона, что приведет к образованию олефина. Так, при действии гидроксил-аниона на катион ( V) вместо ожидаемого трет. [19]
Анион Y -, обычно обладает не только нуклеофильными, но и основными свойствами и может отщепить водород от f5 - углеродного атома карбокатиона, что приведет к образованию олефина. Так, при действии гидроксил-аниона на катион ( V) вместо ожидаемого трет. [20]
Подобно СЩВ данный способ основан на внутрипластовом образовании упругих дисперсных фаз на путях фильтрации пластовой воды за счет ее взаимодействия с микрооторочками закачиваемых в пласт ЩПР. При взаимодействии с породой свободных гидроксил-анионов щелочи в минерализованной пластовой воде происходит деструктурирование адсорбционных слоев нефти и улучшение смачиваемости нефтенасыщенной породы водой. С другой стороны, щелочная среда может за счет снижения межфазного натяжения изменять структурно-механические свойства нефти и приводить к ее диспергированию. [21]
Реакция протекает так, что гидроксил атакует углеродный атом со стороны, противоположной той, где находился атом брома. Одновременно с завязыванием связи между углеродным атомом и гидроксил-анионом происходит ослабление связи между углеродом и бромом. После образования связи углерод - кислород связь углерод - бром полностью разрывается. [22]
Механизм реакции Канниццаро сходен с механизмом реакции Меервейна - Понндорфа. В циклическом переходном состоянии, образованном двумя молекулами альдегида, гидроксил-анионом и катионом щелочного металла, происходит перенос атома водорода со связывающими электронами от одной молекулы альдегида к другой молекуле. [23]
Макрорадикал инициирует привитую полимеризацию мономера, а гидроксил-радикал диффундирует в раствор мономера, вызывая образование гомополимера. Если в растворе находятся ионы ме таллов переменной валентности, то гидроксил-радикал восстанавливается до гидроксил-аниона и возможность образования гомополимера значительно уменьшается. [24]
Все проведенные здесь рассуждения о влиянии природы растворителя и основания на ход реакции в общем согласуются с экспериментальными данными. Выходы олефинов обычно выше при проведении реакции с этилат-анионом в этаноле, чем с гидроксил-анионом в воде. [25]
Единственным примером алкена, обладающего достаточной активностью, чтобы вступать в нуклеофильные реакции всех типов, является этиловый эфир бензилиден-циануксусной кислоты. В определенных условиях к этому соединению присоединяется цианистый водород или бисульфит натрия; оно расщепляется водой или гидроксил-анионами, обменивает группу C ( CN) COOC2HS на группу C ( CN) 2, образует цвиттер-ион с фосфинами, вступает в нуклеофильную димеризацию и нуклеофильную изомеризацию. Очевидно, что такое обилие превращений усложняет кинетические исследования, изучение механизмов и даже препаративное применение этих реакций. [26]
Единственным примером алкена, обладающего достаточной активностью, чтобы вступать в нуклеофильные реакции всех типов, является этиловый эфир бензшшден-циануксусной кислоты. В определенных условиях к этому соединению присоединяется цианистый водород или бисульфит натрия; оно расщепляется водой или гидроксил-анионами, обменивает группу C ( CN) COOC2H6 на группу C ( CN) 2, образует цвиттер-ион с фосфинами, вступает в нуклеофильную димеризацию и нуклеофильную изомеризацию. Очевидно, что такое обилие превращений усложняет кинетические исследования, изучение механизмов и даже препаративное применение этих реакций. [27]
Схема (6.74) позволяет предвидеть, какой именно остаток предпочтительно перемещается при перегруппировке несимметричных бензильных производных. Если фенильная группа содержит - / - или - Af-заместитель, то нуклеофильность соседнего карбонильного углерода повышается, гидроксил-анион или алкоксил-анион присоединяется преимущественно по этому месту и вытесняет соответствующий фенил ьный остаток. [28]
Изменение условий реакции также может влиять на выход олефина. Роль основания в реакции обычно выполняет основание, сопряженное с растворителем, которое образуется при отщеплении протона от молекулы растворителя. Например, гидроксил-анион является сопряженным основанием с молекулой воды, а этилат-анион - с этиловым спиртом. Любое изменение растворителя приводит к изменению природы основания. [29]
Первичные алифатические амины подвергаются дезаминирова-нию с выделением азота и образованием спиртов или непредельных углеводородов. Реакция идет через промежуточно образующееся дйазосоедйнение ( в примере - пропилдиазонийхлорид), от которого отщепляется азот с образованием карбкатиона. Стабилизация последнего осуществляется разными путями: присоединяя гидроксил-анион ( из воды), карбкатион превращается в спирт, а теряя протон, - в непредельный углеводород. [30]
Страницы: 1 2 3