Гидроксил-ион
Cтраница 3
Таким образом, концентрация гидроксил-ионов, происходящих от свободной основной группы, сильно понижается. [31]
Очистку хлорида калия от гидроксил-ионов осуществляют возгонкой КС1 из расплава и продувкой расплава сухим хлористым водородом. [32]
Определение основано на реакции гидроксил-иона со смешанным кислотно-основным индикатором и последующем фотометрировании окрашенного продукта. [33]
В области этих концентраций гидроксил-ионов смещение, по-видимому, линейно. Точное измерение изменения коэффициента невозможно из-за медленного разложения вещества. Это уменьшение поглощения при данной концентрации гидроксил-ионов в зависимости от времени было проверено определением продуктов разложения с помощью иодо-колориметрии. Ультрафиолетовые спектры поглощения, титрование и данные разложения наводят на мысль о присутствии одного или более видов заряженных частиц в щелочных растворах. [34]
При действии на зону гидроксил-иона раствором азотнокислого серебра она делается коричневой вследствие образования гидрата окиси серебра; от действия железо-аммиачных квасцов - красно-коричневой и от действия тимолсинего-синей. [35]
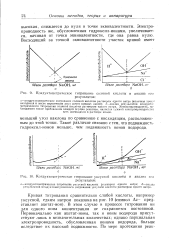
Выше рН 6 недостаток гидроксил-ионов уже не является фактором, ограничивающим скорость гелеобразования. На рис. 4.13 схематически показано возрастание каталитического воздействия гидроксил-ионов с увеличением рН и уменьшение числа эффективных столкновений между частицами с повышением рН и с возрастанием заряда на частицах. [36]
Хлористый метилен реагирует с гидроксил-ионом по Зк2 - механизму значительно менее энергично, чем хлористый метил. При реакции образуется хлорметанол, который претерпевает быструю реакцию Е2 - отщепления, образуя формальдегид - вещество, которое существует в водном растворе главным образом в виде диоксиметана. [37]
Хлористый метилен реагирует с гидроксил-ионом по 8к2 - ме-ханизму значительно менее энергично, чем хлористый метил. При реакции образуется хлорметанол, который претерпевает быструю реакцию Е2 - отщепления, образуя формальдегид - вещество, которое существует в водном растворе главным образом в виде диок-симетана. [38]
Хлористый метилен реагирует с гидроксил-ионом по Зк2 - механизму значительно менее энергично, чем хлористый метил. При реакции образуется хлорметанол, который претерпевает быструю реакцию Е2 - отщепления, образуя формальдегид - вещество, которое существует в водном растворе главным: образом в виде диоксиметана. [39]
В противоположность реакциям с гидроксил-ионами оптически активные бензилфосфониевые соли дают почти полностью. [40]
Электропроводность же, обусловленная гидроксил-ионами, увеличивается, начиная от точки эквивалентности, где она равна нулю. [41]
Взаимодействие бромистого нитрометил-трифенилфосфония с гидроксил-ионом приводит к образованию окиси трифенилфосфина и фульминат-иону. [42]
 |
Кондуктометрическое титрование уксусной. [43] |
Электропроводность же, обусловленная гидроксил-ионами, увеличивается, начиная от точки эквивалентности, где она равна нулю. [44]
Разрыв С-0-связи с прямым вытеснением гидроксил-ион в спиртах термодинамически крайне невыгоден [31] Однак V У Са-атома при наличии свободного фенольного гидроксила и-положении подобный тип превращения становится возможным так как кислород фенолят-иона, являясь мощным донором эле тронов, создает электронное давление на Са-0 - связь, значительн облегчая ее разрыв При этом, очевидно, образование сравнител. [45]
Страницы: 1 2 3 4