Свободный гидроксиламин
Cтраница 1
Свободный гидроксиламин и его щелочные растворы восстанавливают некоторые хиноны до гидрохинонов. Отдельные хиноны восстанавливаются также солянокислым гидроксиламииом. Бензохинон восстанавливается свободным гидроксиламином до гидрохинона. [1]
Свободный гидроксиламин получают из его солей при обработке основаниями. При нагревании, например при перегонке в вакууме, гидроксиламин может разлагаться с оглушительным взрывом на аммиак, азот, окись азота ( 1) и воду. Поэтому обычно применяют соли гидро-ксиламина, которые безопасны. [2]
Вместо свободного гидроксиламина часто можно применять смесь соли гидроксил-амина с рассчитанным количеством гидроокиси щелочного металла [ см. примечание 48, стр. Часто, особенно в ароматическом ряду, в нейтральном или щелочном растворе образуются ос-оксимы, а в солянокислой среде-стереоизомерные им - оксимы. Ниже приводим несколько примеров таких синтезов. [3]
Так как свободный гидроксиламин сравнительно малоустойчив на воздухе, его почти всегда используют в виде соли. [4]
При нагревании свободный гидроксиламин распадается со взрывом: при нагревании открытым огнем в пробирке очень небольшого его количества происходит оглушительный взрыв. Раствор гидр окси л амина имеет сильно щелочную реакцию. [5]
Этим достигаются непрерывное выделение из соли свободного гидроксиламина, расходуемого на оксимирование, нейтрализация сульфата оксима с выделением его в виде второй жидкой фазы и, следовательно, достаточная степень превращения реагентов. [6]
Оксим а-камфенона получен взаимодействием кетона со свободным гидроксиламином в растворе метилового спирта и перекристаллизован из смеси спирта с хлороформом. [7]
При взаимодействии солянокислого гидроксиламина с содой образуется свободный гидроксиламин NH2OH, имеющий темп. [8]
Оксимирование в этом случае также протекает со свободным гидроксиламином. Изменение основности реакционной смеси по окончании оксимирования определяют титрованием хлорной кислотой в неводной среде. [9]
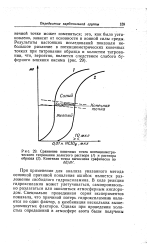 |
Сравнение конечных точек потенциометри. [10] |
При применении для анализа указанного метода основной причиной появления ошибок является разложение свободного гидроксиламина. В ходе реакции гидроксиламин может улетучиваться, самопроизвольно разлагаться или окисляться атмосферным кислородом. Специально проведенная серия экспериментов показала, что причиной потерь гидроксиламина является не один фактор, а комбинация нескольких вышеупомянутых факторов. [11]
При применении для анализа указанного метода основной причиной появления ошибок является разложение свободного гидроксиламина. В ходе реакции гидроксиламин может улетучиваться, самопроизвольно разлагаться или окисляться атмосферным кислородом / Специально проведенная серия экспериментов показала, что причиной потерь гидроксиламинпа является не один фактор, а комбинация нескольких выше упомянутых факторов. [12]
Для определения карбонильной группы применялся 0 06 - 0 08 н ( относительно свободного гидроксиламина) раствор, в котором 0 2 м спиртовой раствор солянокислого гидроксиламина наполовину нейтрализован спиртовым раствором едкого калия. [13]
Полученный раствор не очень устойчив, но все же более стоек, чем свободный гидроксиламин. Реакция оксимирования при использовании такого раствора протекает со свободным гидроксиламином. [14]
Необходимо довольно тщательно контролировать рН реакционной смеси, так как для реакции требуется свободный гидроксиламин ( который образуется в момент выделения) и в возникающей при этом щелочной среде возможно омыление амидов. [15]
Страницы: 1 2 3