Гидроксилапатит
Cтраница 3
Степень разложения фосфата ( гидроксилапатита) для отдельных точек на кривых растворимости определяется по проходящей через них линии степени нейтрализации ( лучу растворения) при помощи верхней части диаграммы. Пример графического определения коэффициента разложения фосфорной кислотой концентрации 40 % Р2О5при1000 ( для узловой точки при 100) показан тонким пунктиром. Из положения узловых точек Е видно, что степень нейтрализации жидкой фазы, а следовательно, и коэффициенты разложения в этих точках близки к максимуму для каждой температуры. [31]
Предшествующие опыты показали, что гидроксилапатит стабилизируется в присутствии водяного пара в газовой фазе. При рассмотрении влияния кремнезема на суммарный процесс обес-фторивания было установлено, что небольших добавок кремнезема к фторапатиту достаточно, чтобы вызвать интенсивное превращение обесфторенного продукта в лимоннорастворимую форму. [32]
При кристаллизации двухзамещенного фосфата кальция гидроксилапатит остается в виде слизистых хлопьев. [33]
R, которая соответствует составу гидроксилапатита. Замена фторапатита гидроксилапатитом допустима [22 - 25], если не учитывать образования фтористого водорода. [34]
При 70 С луч растворения гидроксилапатита пересекает кривую растворимости двухзамещенного фосфата кальция. [35]
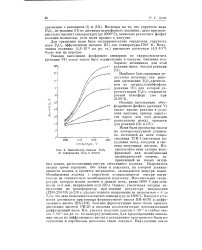 |
Зависимость выхода Ра от содержания SiCb в шихте. [36] |
Реакция вытеснения фосфорного ангидрида из гидроксилапатита ( реакция VI) также может быть осуществлена в вакууме. [37]
Фторапатит заменен в данном случае гидроксилапатитом, так как предположено. [38]
Известно, что водяной пар стабилизирует гидроксилапатит, поэтому нами было высказано следующее предположение: при медленном охлаждении в присутствии водяного пара происходит образование гидроксилапатита, приводящее к снижению лимоннорастворимости. Такое заключение нуждается в разносторонней проверке, поэтому мы исследовали процесс образования гидроксилапатита при высокотемпературном взаимодействии шихт, состоящих из трикальцийфосфата и окиси кальция, с водяным паром при 900 С. [39]
Примером этому может служить кальциевый или стронциевый гидроксилапатит. Двузамещенный фосфат бария является исключением в том отношении, что он гидролизуется с переходом в Ваз ( Р04) а [26] чрезвычайно медленно. Основной фосфат магния имеет моноклинную кристаллическую структуру, которая отличается от гексагональной структуры кристаллов апатита. Клемент [27] показал, что трехза-мещенный фосфат магния при обработке водой гидролизуется с образованием промежуточного основного фосфата, который претерпевает дальнейший гидролиз до гидратированной окиси магния. [40]
Фазовому рентгеноструктурному анализу были подвергнуты образцы гидроксилапатита, прокаленного в токе сухого воздуха при 1350 С и в тех же условиях, с добавкой 5 % кремнезема. [41]
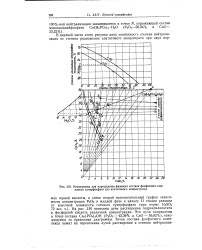 |
Номограмма для определения фазового состава фосфатного комплекса суперфосфата ( из апатитового концентрата. [42] |
На рис. 210 нанесены лучи растворения гидроксилапатита в фосфорной кислоте различной концентрации. Эти лучи направлены в точку состава Са5 ( РО4) зОН ( Р2О5 - 42 39 % и СаО - 55 82 %), находящуюся за пределами диаграммы. [43]
При фильтровании воды с большим содержанием фтора гидроксилапатит действует как селективный анионит, так как происходит обмен гидроксиль-ных ионов сорбента на ионы фтора. Гидроксилапатит регенерируют 1 % - ным раствором гидроксида натрия; его расход составляет 100 г на 1 г поглощенного Гидроксилапатитом фтора. [44]
R, которая соответствует со-ст & ву гидроксилапатита. Замена фторапатита гидроксилапатитом допустима [22 - 25], если не учитывать образования фтористого водорода. [45]
Страницы: 1 2 3 4