Гидроксилирова-ние
Cтраница 1
Гидроксилирова-ние и гликозилирование дают растворимые соединения, значение которых в жизни растения не так ясно, как значение лигнина, но которые, вероятно, приносят некоторую пользу по крайней мере тем, что привлекают насекомых для опыления. Рассматривается тот же общий процесс эволюции - мутации, дающие новые продукты, которые могут действовать благодаря существующим ферментам и обусловливают преимущества мутантов по сравнению с исходным штаммом; за этими мутациями следуют другие полезные мутации. [1]
Свободнорадикальное гидроксилирова-ние ароматических соединений представляет большой интерес в связи с биологическими процессами гидроксилирования; множество реагентов было использовано для имитации действия многофункциональных оксидаз. Синтетическая ценность таких систем ограничена низкими выходами образующихся оргоДшра - продуктов. [2]
 |
Молекулярные модели кортикостероида ( А и карденолида ( Б. [3] |
На протекание ферментативного гидроксилирова-ния существенное влияние оказывают уже имеющиеся в субстрате оксигруппы. Прежде всего их влияние сказывается на общей активности гидроксилаз - гидроксилирование идет наиболее быстро в том случае, если субстрат совсем не содержит оксигрупп; монооксисоединения трансформируются заметно медленнее а ди - и триоксисоединения гидроксилируются очень плохо. Исключение, однако, составляет гидроксилирование в положения 1а, 2, 16а и 19; которое протекает с заметной скоростью даже с такими полигидроксили-рованными субстратами, как кортизол и его 16а - оксипроизводное, хотя последнее содержит даже четыре оксигруппы ( см. гл. [4]
Роль дигидробиоптерина в ферментативном гидроксилирова-нии фенилаланина стала более ясной в результате изящных работ Кауфмана [44], из которых следует, что в этом процессе принимают участие три фермента. В связи с этим предполагается, что тетрагидропроизводное ( 45) и является природным коферментом, в то время как 7 8-дигидропроизводнос представляет собой артефакт, образующийся в процессе выделения, а ферментативное восстановление по схеме ( 32) - спасательный механизм. [5]
Эпоксидирование в индифферентном растворителе или гидроксилирова-ние в кислой среде требуют сравнительно сильноосновного олефина ( этилен, замещенный алкильными или арильными группами), а р - Ненасыщенные кетоны или альдегиды в этих условиях не реагируют, но могут быть эпокси-дированы перекисью водорода в слабощелочной среде. [6]
Сюда относятся, например, реакции гидроксилирова-ния, аминирования. [7]
Если R Gl, CHg, OH, C6H5, S03K или Н, то гидроксилирова-ние не протекает, а имеет место лишь окисление в соответствующие бензохиноны. Образовавшиеся в результате реакции (10.35) три-гидроксисоединения не являются стабильными продуктами, а под - вергаются дальнейшему электрохимическому окислению в соответствующие оксихиноны. [8]
Если R Cl, CH3, OH, CeH5, S03K или Н, то гидроксилирова-ние не протекает, а имеет место лишь окисление в соответствующие бензохиноны. Образовавшиеся в результате реакции (10.35) три-гидроксисоединения не являются стабильными продуктами, а подвергаются дальнейшему электрохимическому окислению в соответствующие оксихиноны. [9]
Для объяснения ( Механизма окисления парафина были предложены три главных теории: 1) окисление протекает в соответствии с теорией гидроксилирова-ния; 2) углеводороды1 отщепляют во время нагревания водород и становятся ненасыщенными, и окисление происходит по двойной связи, сопровождаясь разрывом молекулы; 3) сначала происходит образование эфиров, за которым. [10]
Аналогичное действие оказывает на ненасыщенные соединения, по-видимому, также и газообразный кислород в присутствии мелко раздробленного металлического есмия, но этот способ гидроксилирова-ния изучен преимущественно при окислении олефинов 9В6 ( см. XVI, 2, стр. [11]
Райли нашел, что селенистая кислота окисляет группу - СН2СО - до - COCO - ( это превращение называют реакцией Райли); при действии селенистой кислоты происходит также аллильное гидроксилирова-ние и дегидрирование. [12]
При действии на фенолы пероксодисульфата калия ( или аммония) в щелочном растворе в молекулу вступает группа OSO & K, а последующий гидролиз в кислой среде приводит к двухатомным фенолам ( реакция Эльбса), Так, при постепенном добавлении насыщенного водного раствора К Ов к раствору моногид-роксисоединения в 10 % - м водном растворе NaOH при температуре не выше 20 С и последующем подкис лении из фенола ( 12) получают гидрохинон ( 19) ( выход 34 %), из о-хлорфе-нола - 2-хлоргидрохинон ( 62 %) [689], из пиридона-2 - 5-гид-роксипиридон - 2 ( 42 %) [ 424, с. Реакция гидроксилирова-ния фенолов по Эльбсу ускоряется при наличии электронодо-норных и замедляется при наличии электроноакцепторных заместителей, имеет общий второй порядок ( первый по субстрату и по пероксодисульфат-дианиону), нечувствительна к ингиби-лорам радикальных реакций. [13]
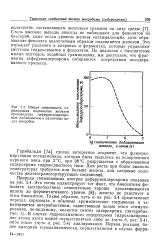 |
Общая зависимость, отражающая подавление железом производства деферрисидерохро-мов, наблюдаемое в различных видах микробов. [14] |
Природа связывающих центров деферрисидерохрома показана на рис. 5.4. Зта схема иллюстрирует тот факт, что биосинтезы фенолята ( энтеробактина) относительно хорошо прослеживаются вплоть до ферментативного уровня [8]; железо не участвует в этом биосинтезе. В случае гидроксаматного сидерохрома гидроксилирова-ние атома азота может осуществляться либо до ( путь б, рис. 5.4), либо после ( путь в, рис. 5.4) ацилирования. [15]
Страницы: 1 2