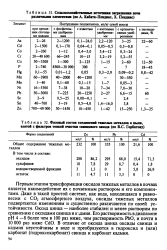
Гидроксокарбонат
Cтраница 3
Схема производства сводится к следующим операциям. В горячем паровом конденсате при t л; 70 - 90 С в течение 30 мин растворяют нитрат никеля и оксид бария. В шнековом смесителе ведут 15 - 20 мин сухое перемешивание дозированных количеств гидроксокарбоната никеля, прокаленного оксида магния и гидро-ксида либо оксида алюминия. Далее в смеситель поступают растворы нитрата никеля и оксида бария, и совместное перемешивание компонентов продолжается еще 50 - 60 мин. [31]
Магний, относящийся ко II группе периодической системы, во всех соединениях имеет степень окисления 2 и отличается от остальных катионов 1 - й аналитической группы рядом свойств. Так, гидроксид магния плохо растворим в воде и является довольно слабым основанием. Ион Mg2 является переходным между катионами 1 - й и 2 - й аналитических групп. Гидроксокарбонат магния ( М § ОН) 2СОз, подобно карбонатам катионов 2 - й группы, мало растворим в воде. Однако он растворяется в избытке солей аммония и при действии карбонатом аммония в присутствии хлорида аммония не выпадает в осадок. Поэтому ион Mg2 остается в растворе с катионами 1 - й группы. [32]
Основные соли могут быть получены различными методами, которые обычно включают - непосредственно или косвенно - гидролиз обычной соли. Гидролиз может быть проведен в условиях контролируемой температуры, кислотности и концентрации ионов металла либо ( косвенно) путем нагревания гидрата соли. Многие Гидроксосоли получаются в результате последнего процесса вместо обычных безводных солей, например Cu2 ( OH) 3NO3 образуется при нагревании гидрата нитрата меди. Осадки, образующиеся при добавлении раствора карбоната натрия к растворам солей металлов, как правило, представляют собой гидроксокарбонаты. Некоторые металлы не образуют нормальных карбонатов ( например, медь; см. разд. [33]
Первым этапом трансформации оксидов тяжелых металлов в почвах является взаимодействие их с почвенным раствором и его компонентами. Даже в такой простой системе, как вода, находящаяся в равновесии с СО2 атмосферного воздуха, оксиды тяжелых металлов подвергаются изменениям и существенно различаются по своей устойчивости. Оксид цинка - наиболее стабилен и менее растворим по сравнению с оксидами свинца и к хцмия. В отличие от оксида цинка оксиды свинца и кадмия неустойчивы в воде и преобразуются в гидроксид и ( или) карбонат ( гидроксокарбонат) свинца и карбонат кадмия. [35]
Страницы: 1 2 3