Гидроксокомплекс
Cтраница 2
Образование гидроксокомплексов заметно уменьшает период полуобмена воды, координированной в аквакомплекс [ 40, гл. [16]
Формы гидроксокомплексов: М: ц ( он) 4 и ZNifcOH5 1 определены в растворах при температурах: О, 25, НО, 60, 80, 100, 125, 150 С. Комстаиты гидролиза с повышением температуры увеличиваются. Повышение температуры способствует образованию свободных молекул воды в растворе, увеличению констант диссоциации воды [ l ] усилению гидролитических реакций. [17]
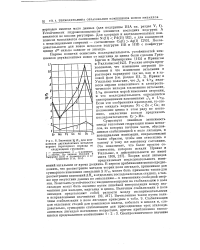 |
Значения lg Кг для комплексов двухвалентных металлов первого переходного периода со следующими группами. [18] |
Устойчивости гидроксокомплексов элементов последних подгрупп А меняются не вполне регулярно. Последовательности для ионов металлов подгрупп ИВ и П1В с конфигурациями dw сильно зависят от лиганда. [19]
Если присутствуют гидроксокомплексы, то нижнее предельное значение / отрицательно. Если в распоряжении имеется достаточный набор экспериментальных данных В, Н, A, b, h, а, то уравнения ( 18 - 1), ( 18 - 2) и ( 18 - 3) можно в принципе решить относительно констант устойчивости. Однако без использования электронной вычислительной машины этот метод крайне трудно применить к системам, в которых присутствует более одного или двух комплексов неизвестной устойчивости. [20]
Даже если никакие гидроксокомплексы и не образуются, во многих полуреакциях принимают участие ионы водорода или гидр-оксильные ионы, и для них потенциал должен зависеть от кислотности раствора и от концентрации других частиц. [21]
Константа равновесия гидроксокомплекса, определяемая уравнением ( 2 4), является константой диссоциации комплекса, как кислоты, и тогда определяется аналогичным образом из кривой титрования. [22]
Установлено образование гидроксокомплексов с константами равновесия, рассчитанными по методу диализа. [23]
Кристаллические осадки гидроксокомплексов и их водные растворы энергично взаимодействуют с СО2, SO2, H2S и другими веществами, обладающими кислотными свойствами. [24]
Выявление полимеризации гидроксокомплексов привело к формированию нового раздела координационной химии - химии неорганических гидроксополимеров, которые характерны [10] для большинства гидратированных ионов металлов за исключением щелочных и Са, Sr, Ba. Это открывает широкие перспективы для поиска, и разработки новых неорганических клеев. Поскольку гидроксополимеры различных металлов отличаются по форме, структуре, заряду, клеи на их основе могут иметь широкую гамму свойств. [25]
 |
Влияние рН на. [26] |
Образование полиядериых гидроксокомплексов характерно для Al3, ZrIV, HfIV, Be2 и других элементов. [27]
Выявление полимеризации гидроксокомплексов привело к формированию нового раздела координационной химии - химии неорганических гидроксополимеров, которые характерны [10] для большинства гидратированных ионов металлов за исключением щелочных и Са, Sr, Ba. Это открывает широкие перспективы для поиска, и разработки новых неорганических клеев. Поскольку гидроксополимеры различных металлов отличаются по форме, структуре, заряду, клеи на их основе могут иметь широкую гамму свойств. [28]
В системах гидроксокомплексов индия [5] и олова ( II) [99] ( см. рис. 83) значения g ( u), полученные из измерений со стеклянным и с амальгамным электродами, хорошо согласуются. [29]
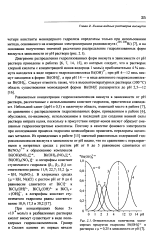 |
Относительные количества мономерных продуктов гидролиза Bi ( OH в растворах с ц 0 25 в зависимости от рН. [30] |
Страницы: 1 2 3 4