Гидроксохлорид
Cтраница 1
 |
Кристаллическая структура Mg2 ( OH 3Cl - 4 Н2О. [1] |
Гидроксохлорид РЬС1 ( ОН) встречается в природе в виде минерала лаурионита. Его структура очень похожа на структуру РЬС12 ( разд. [2]
Гидроксохлорид рутения представляет собой темно-коричневый порошок, растворимый в хлороводородной кислоте. В воздухе присутствует в виде аэрозоля. [3]
Для гидроксохлоридов циркония наблюдаемые в интервале 170 - 250 С эндоэффекты вызваны удалением кристаллизационной воды. Экзоэффект при 280 С объясняется кристаллизацией связки и дальнейшим удалением воды. [4]
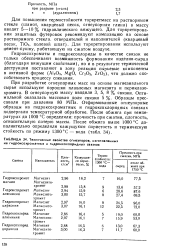 |
Технические свойства огнеупоров, изготовленных на гидроксохроматных и гидроксохлоридных связках. [5] |
Гидроксохроматы и гидроксохлориды в качестве связок не только обеспечивают возможность формования изделия-сырца ( благодаря вяжущим свойствам), но и в результате термической деструкции поставляют в зону реакции сырьевые компоненты в активной форме ( AI2O3, MgO, Cr2O3, ZrO2), что должно способствовать процессу спекания. [6]
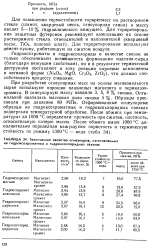 |
Технические свойства огнеупоров, изготовленных на гидроксохроматных и гидроксохлоридных связках. [7] |
Гидроксохроматы и гидроксохлориды в качестве связок не только обеспечивают возможность формования изделия-сырца ( благодаря вяжущим свойствам), но и в результате термической деструкции поставляют в зону реакции сырьевые компоненты в активной форме ( А1гОз, MgO, Сг2Оз, ZrOz), что должно способствовать процессу спекания. [8]
При использовании гидроксохлоридов в зависимости от характера порошков наблюдается различное их взаимодействие: для шамота и кварцевого стекла - преимущественно адгезионное, а для магнезиальных порошков - химическое. Переход гидроксо-хлорида в нерастворимое состояние в алюмосиликатных и кварцевых шихтах происходит под действием температуры, точно так же, как и у исходного гидроксохлорида. В присутствии магнезиальных порошков гидроксохлорид разлагается. [9]
Важное промышленное значение имеет гидроксохлорид магния MgOHCl. Технический продукт получается путем замешивания оксида магния с концентрированным водным раствором хлорида магния и носит название магнезиального цемента. Такая смесь через некоторое время затвердевает, превращаясь в плотную белую, легко полирующуюся массу. [10]
Так, получаемые в процессе пере-алюминийсодержащих отходов гидроксохлориды алю-могут заменить сульфат алюминия при очистке воды оборотных систем нефтеперерабатывающих и нефтехимических предприятий, в производстве огнеупоров, строительной керамики, фарфора, вяжущих веществ, бумаги и картона, очистке теп-оборудования от карбонатных отложений. До времени практически все отходы, получаемые при использовании безводного хлорида алюминия ( производства этилбензола, изопропилбензола, синтетических спиртов, присадок и др., где в качестве катализатора реакций Фриделя - Крафтса - Густавсона используют хлорид алюминия) сбрасывали в отвал. На обработку алюминийсодержащих кислых и сточных вод потребляется значительное количество I, серной кислоты и других дефицитных реагентов. Кубовые остатки, получаемые в различных нефтехимических производствах, почти не находят квалифицированного применения. Однако они содержат ценные органические соединения, которые могут быть использованы в различных областях народного хозяйства. Так, на Стерлитамакском опытно-промышленном нефтехимическом заводе, сжигавшиеся ранее кубовые остатки ректификации 2 6-ди-грег - бутилфенола и регенерации метанола после его использования для перекристаллизации ионола, сейчас используют для производства доступных и эффективных антиокислительных присадок для автомобильных бензинов. [11]
Сравнительно прост в приготовлении сульфаматный электролит, получаемый из гидроксохлорида рутения. В нем осаждаются рутениевые покрытия толщиной до 12 мкм. [12]
Полученные ИК-спектроскопические данные коррелируют с данными ДТА, но при постадийном нагревании разложение собственно гидроксохлорида происходит при более низкой температуре - 150 - 170 С, как на деризатограмме. Следовательно, термическое превращение ГХА зависит не только от температуры, но и от режима его термообработки. [13]
 |
Номенклатура кислот и их средних солей. [14] |
Названия основных солей образуют аналогичным образом, добавляя приставку гидроксо -: ( СиОН СОз - гидроксокарбонат меди, Mg ( OH) Cl - гидроксохлорид магния. [15]
Страницы: 1 2