Гидролиз - бром
Cтраница 1
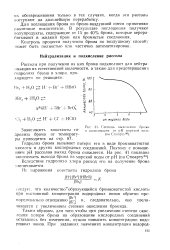 |
Степень выделения брома. [1] |
Гидролиз брома вызывает потери его в виде бромноватистой кислоты и других кислородных соединений. Поэтому с повышением рН рассолов выход брома снижается. [2]
 |
Технологическая схема извлечения брома из рапы методом. [3] |
Гидролиз брома предотвращается в большей своей степени предварительным подкислением рапы. [4]
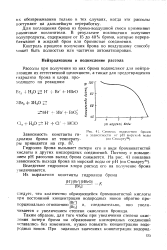 |
Степень выделения брома. [5] |
Гидролиз брома вызывает потери его в виде бромноватистой кислоты и других кислородных соединений. Поэтому с повышением рН рассолов выход брома снижается. [6]
Константа гидролиза брома с повышением температуры увеличивается, поэтому при высоких температурах потери брома в результате гидролиза будут больше, чем при низких. [7]
Скорость гидролиза брома определяется при прочих равных условиях концентрациями в растворе щелочи и брома и скоростью их диффузии. Поэтому при малой Сщ, вогда в жидкой фазе сосредоточена значительная доля сопротивления массопередачи, в. При большой концентрации На ОИ процесс в жидкой фазе протекает мгновенно - отсутствует стадия накопления брома. Комплевсообразование брома в растворе по реакции Ь-12 ва гг & чз - также снижает спорость абсорбции. Влияние комплевсообразования возрастает с повышением Сг и Wf. Повышение вонцентрации бромида в сорбенте способствует увеличению доли закомплексованного брома, что хорошо согласуется с полученными нами результатами по уменьшению величины К F с возрастанием концентрации бромных солей. Увеличение роли комплексообразования в суммарном процессе щелочной абсорбции брома должно приводить в возрастанию относительной доли сопротивления жидкой фазы в процессе массопередачи. [8]
Константа гидролиза брома с повышением температуры увеличивается, поэтому при высоких температурах потери брома в результате гидролиза будут больше, чем при низких. [9]
Зависимость константы гидролиза брома от температуры приводится на стр. [10]
Следовательно, для предотвращения гидролиза брома концентрация водородных ионов должна быть тем больше, чем выше желательная степень окисления, чем ниже концентрация брома в рассоле и чем выше температура. Наоборот, при меньшей степени окисления, при более высокой концентрации брома и при низкой температуре требуется меньшее подкисление. [11]
С уменьшением величины рН рассолов гидролиз брома ослабевает, а выход брома при хлорировании увеличивается. [12]
Она значительно ниже, чем константы гидролиза брома и хлора. [13]
Рассол подкисляют серной кислотой для нейтрализации природной щелочности и подавления гидролиза брома и хлора. Степень подкисления зависит от температуры рассола; чем выше температура, тем сильнее гидролиз галоидов и тем большая кислотность необходима для его подавления. Подкисленный рассол хлорируют до образования хлористого брома, при этом на один эквивалент брома вводят два эквивалента хлора. [14]
Возможность этого обусловлена тем, что константа гидролиза иода значительно меньше констант гидролиза брома и хлора; степень гидролиза иода не велика даже в нейтральных растворах, и следовательно, из них также можно извлекать иод. Процесс извлечения идца после его выделения под действием окислителя нужно осуществлять как можно быстрее, так как при стоянии концентрация иода в нейтральном растворе быстро снижается. Имеются указания1, что концентрация свободного иода в естественной буровой воде за 5 мин. По-видимому, это объясняется расходованием иодноватистой кислоты HJO, являющейся, как известно, более энергичным окислителем, чем иод, на окисление органических примесей буровой воды или превращение ее в иодат. [15]
Страницы: 1 2