Гидролиз - бром
Cтраница 2
Возможность этого обусловлена тем, что константа гидролиза иода значительно меньше констант гидролиза брома и хлора; степень гидролиза иода не велика даже в нейтральных растворах, и следовательно, из них также можно извлекать иод. Процесс извлечения иода после его выделения под действием окислителя нужно осуществлять как можно быстрее, так как при стоянии концентрация иода в нейтральном растворе быстро снижается. Имеются указания1, что концентрация свободного иода в естественной буровой воде за 5 мин. По-видимому, это объясняется расходованием подноватистой кислоты HJO, являющейся, как известно, более энергичным окислителем, чем иод, на окисление органических примесей буровой воды или превращение ее в иодат. [16]
Скорость гидролиза для хлорида брома оценивается менее, чем 0 35 мс, что быстрее гидролиза брома и хлора. [17]
При поглощении брома из бромовоздушной смеси раствором едкого натра происходит нейтрализация смеси бромистоводород-ной и бромноватистой кислот, образующихся при гидролизе растворяющегося брома. [18]
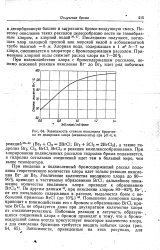 |
Зависимость степени окисления бром-ио - -. [19] |
При хлорировании подкисленных рассолов гидролиз брома подавляется, а гидролиз остальных соединений идет тем в большей мере, чем выше температура. [20]
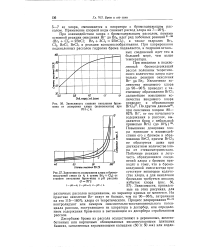 |
Зависимость степени окисления бром-иона от дозировки хлора ( эквиваленты при РН4. [21] |
При взаимодействии хлора с бромсодержащим рассолом, помимо основной реакции окисления Вг - до Bra, идет ряд побочных реакций 21 - 28 ( Вг2 С12 2ВгС1; Вг2 ЗС12 2ВгС13), а также гидролиз Вг2, С12, BrCl, ВгСЬ и реакции комплексообразования. При хлорировании подкисленных рассолов гидролиз брома подавляется, а гидролиз остальных соединений идет тем в большей мере, чем выше температура. [22]
Стабилизирующий эффект, оказываемый наличием второго атома фтора в группе, не ограничивается только этой группой, но распространяется на соседние группы. Например, CH2BrCH2F легко гидролизуется в гликольГ в то время как CH2BrCHFs становится настолько устойчивым, что для гидролиза брома в соседней группе и получения дифторэтилового спирта требуется длительное нагревание с водой и гидраюм окиси ртути при 150 и только при 200 начинается гидролиз фтора с образованием небольшого количества гликольальдегида. В случае CH2FCHF2 атом фтора в группе CH3F более устойчив, чем фтор в фтористом метиле или этиле, что указывает на стабилизирующее действие соседней СНР2 - группы. [23]
Извлечение брома обычно выгоднее производить из рассолов, более богатых бромидами. Но не только содержание брома в исходном сырье определяет экономические показатели процесса; практически очень важными факторами являются температура, соленость, щелочность и состав рассола. Так, при повышении температуры и содержания иона SO -, а также при уменьшении солености ( или при очень большой солености рассола) увеличивается давление пара брома над рассолом и тем самым снижается расход пара или электроэнергии на производство. Повышение щелочности рассола увеличивает расход кислоты, требующейся для подавления гидролиза брома. [24]
Получать бром пз подобных рассолов без подкислення невозможно. Как правило, из них получают одновременно и иод. При этом нейтрализацию щелочи и подкисление осуществляют на стадии получения иода. Щелока калийного производства в большинстве случаев нейтральны. При небольшой щелочности рассолов и высокой концентрации брома их можно не подкислять, так как в природных рассолах всегда содержится большое количество органических и неорганических примесей, при взаимодействии которых с хлором образуется свободная соляная кислота. Таким образом, создается среда, необходимая для подавления гидролиза брома. [25]
Получать бром из подобных рассолов без подкисления невозможно. Как правило, из них получают одновременно и иод. При этом нейтрализацию щелочи и подкисление осуществляют на стадии получения иода. Щелока калийного производства в большинстве случаев нейтральны. При небольшой щелочности рассолов и высокой концентрации брома их можно не подкислять, так как в природных рассолах всегда содержится большое количество органических и неорганических примесей, при взаимодействии которых с хлором образуется свободная соляная кислота. Таким образом, создается среда, необходимая для подавления гидролиза брома. [26]
Страницы: 1 2