Гидролиз - глюкозидная связь
Cтраница 1
Гидролиз глюкозидной связи происходит с обращением аномерной конфигурации аглюкона невосстанавливающего конца целлюлозы или ее фрагментов. Таким образом, серия каталитических актов разрыва глюкозидной связи может продолжаться лишь до появления первого карбоксиметильного заместителя, что сопровождается лишь незначительным образованием восстанавлиявающих Сахаров ( ВС) и сохранением неизменной вязкости раствора КМЦ. [1]
Осахариваиие крахмала до 25 % гидролиза глюкозидных связей [ ротекает как реакция нулевого порядка. [2]
Осахариваиие крахмала до 25 % гидролиза глюкозидных связей протекает как реакция нулевого порядка. [3]
Более вероятно, что значительно меньшая скорость гидролиза глюкозидных связей между звеньями, находящимися в упорядоченных участках, объясняется повышенной устойчивостью глюкозидных связей в макромолекуле целлюлозы к действию кислот, обусловленную влиянием водородных связей во. [4]
Кислоты вызывают значительное уменьшение степени полимеризации целлюлозы в результате гидролиза глюкозидных связей между глюкоз - ными остатками. [5]
Специфичность относительно аглюкона, несомненно, не может быть объяснена только влиянием химических групп в молекуле аглюкона на скорость гидролиза глюкозидной связи. Из рассмотрения рис. 1 видно отсутствие соответствия между кислотным гидролизом ряда ароматических р-глюкозидов и их энзиматическим гидролизом посредством Р - ГЛЮКОЗИДЭЗЫ. Аналогично этому наблюдалось отсутствие подобного соответствия и в случае алкил-глюкозидов, у которых скорость знзиматического гидролиза варьирует в широких пределах, в то время как скорость кислотного гидролиза является почти постоянной. Далее, относительная скорость энзиматического гидролиза р-глюкозидов сильно изменяется в случае применения энзимов из различных источников. [6]
На различных этапах первой фазы расщепления органических соединений выделяется очень мало энергии; Расчеты показывают, что свободная энергия гидролиза глюкозидной связи крахмала составляет около 4 3 ккал, пептидной связи белков - около 3 0 и сложноэфирной связи жиров - около 2 5 ккал на 1 грамм-молекулу. [7]
Холодные разбавленные растворы кислот практически не действуют на ацетатные волокна, а в горячих растворах идет омыление сложноэфирных групп и гидролиз глюкозидных связей, сопровождающийся снижением степени полимеризации макромолекул и уменьшением прочности волокна. [8]
Многие из вышеупомянутых закономерностей являются подтверждением теории о том, что доступность исходной целлюлозы определяет место, в котором происходит неупорядоченный гидролиз глюкозидных связей при приготовлении гидроцеллюлоз. [9]
Отсутствие обращения аномерной конфигурации аглюкона, отсутствие трансгликозилирования и ингибирования глюконолак-тоном позволяет в большинстве случаев предполагать механизм одностадийного 8н2 - замещения при гидролизе глюкозидной связи целлобиогидролазой. При этом вода, атакуя Ci-атом гликона, играет роль нуклеофильного агента, в то время как соответствующая функциональная группа активного центра протонирует глюкозильный кислород, играя роль общекислотного катализатора. [10]
Катализируемый лизоцимом гидролиз глюкозидов является наглядным примером того, как трудно четко разграничить различные типы механизмов реакции и механизмов катализа. Вопрос заключается в том, каким образом взаимодействия с этими группами ведут к увеличению скорости гидролиза глюкозидной связи. [11]
Всеми исследователями [176-178, 196] отмечается значительно меньшая устойчивость сложноэфирной связи в сульфате целлюлозы к кислой среде по сравнению с нейтральной и щелочной. Однако полное отщепление всех сернокислых групп проходит лишь в довольно жестких условиях ( кипячение в НС1) с одновременным гидролизом глюкозидной связи в макромолекуле целлюлозы. Некоторыми из указанных авторов отмечается, что при проведении гидролиза кислотой в метаноле молекулы целлюлозы деструктируются меньше, чем в воде. [12]
При облучении целлюлозы ( или любого из упомянутых выше ее производных) в массе ультрафиолетовым светом при нормальных атмосферных условиях наблюдается быстрое уменьшение вязкости ее растворов, сопровождающееся увеличением ее восстанавливающей способности, измеряемой, например, по медному числу. Уменьшение вязкости растворов указывает на протекание реакции разрыва цепей, а увеличение восстанавливающей способности объясняется образованием потенциальных альдегидных групп в результате гидролиза глюкозидных связей между звеньями. Предположение о том, что эти реакции являются фотогидролизом [39] и что они возможны благодаря присутствию в полимере следов влаги, опровергается результатами последующих работ. Как правило, скорость увеличивается при повышении давления кислорода. [13]
Активность прочно адсорбирующихся ферментов ( независимо от вида специфической активности) ограничена в силу из незначительной подвижности по матрице нерастворимого целлюлозного субстрата. Молекулы прочно адсорбирующихся ферментов относительно быстро гидролизуют реакционноспособный субстрат ( аморфные участки целлюлозы) в локальной зоне своей дислокации, но их транспорт по поверхности субстрата на другую подходящую зону затруднен или происходит медленно. Напротив, слабо адсорбирующиеся ферменты после акта гидролиза глюкозидной связи на поверхности целлюлозы десорбируются в раствор и не испытывают подобных затруднений, проявляя поэтому более высокую активность. Синергизм является следствием того, что слабо адсорбирующиеся ферменты гидролизуют субстрат в зонах дислокации прочно адсорбирующихся ферментов: это приводит к появлению возможности для последних изменить свое положение на субстрате и оказаться на его более реакцион-носпособном участке. [14]
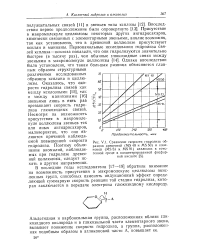 |
Сравнение скорости гидролиза об. [15] |
Страницы: 1 2