Гидролиз - соль - железо
Cтраница 3
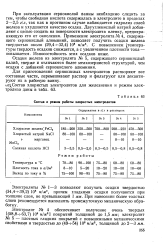 |
Состав и режим работы хлористых электролитов. [31] |
При эксплуатации сернокислой ванны необходимо следить за тем, чтобы свободная кислота содержалась в электролите в пределах 2 - 2 5 г / л, так как в противном случае наблюдается гидролиз солей железа и ухудшается качество осадка. Двууглекислый натрий добавляют с целью создать на поверхности электролита пленку, предохраняющую его от окисления. С повышением [ температуры твердость осадков снижается, а с увеличением плотности тока - повышается. [32]
В процессе транспорта и хранения воды этот показатель может изменяться: рН сероводородных вод увеличивается вследствие выделения сероводорода и СО2, рН железосодержащих вод увеличивается с удалением СОз и уменьшается в результате окисления и гидролиза солей железа. [33]
Несмотря на то что в справочной литературе приводятся величины произведения растворимости для свежих и старых гидроксидов, исследованиями установлено, что полный гидролиз - процесс медленный, и устойчивое состояние равновесия, например при гидролизе солей железа, достигается через пять-шесть месяцев. [34]
При хранении и транспорте хлоркальциевых пластовых вод девона и карбона рН их изменяется: рН сероводородных вод увеличивается вследствие выделения сероводорода и СО2, а рН железосодержащих вод увеличивается с удалением СО2 и уменьшается в результате окисления и гидролиза солей железа. [35]
Рентгенографически установлено, ч-при гидролизе солей железа ( III) в гидрокарбонатно-хлориднь и гидрокарбонатно-сульфатных средах образуется одна и та л модификация гидроксида железа ( III) - гетит a - FeO ( OH Характерно, что a - гидроксид железа ( III) образуется и в ел чае гидролиза солей железа ( II), например, железного купор са, окисляемого хлором или растворенным в воде кислороде при подщелачивании известью. [36]
Удаление примесей железа, меди и цинка обычно осуществляется путем подщелачивания электролита карбонатом или гидроокисью никеля до рН 6 2 - 6 3 с последующим нагревом электролита до температуры кипения. Гидролиз солей железа протекает эффективнее при введении окислителей ( перекись водорода), но окислители нельзя вводить в электролиты, содержащие окисляемые органические блескообразователи. [37]
Получающийся при этом осадок пристает к стенкам стакана, плохо отфильтровывается и отмывается. Чтобы предотвратить гидролиз соли железа, раствор перед нагреванием подкисляют HNO3, которая в процессе осаждения Fe нейтрализуется аммиаком. Образующийся NH4NO3 играет роль электролита-коагулятора. [38]
Получающийся при этом осадок пристает к стенкам стакана, плохо отфильтровывается и отмывается. Чтобы предотвратить гидролиз соли железа, раствор перед нагреванием подкисляют азотной кислотой, которая в процессе осаждения Fe3 нейтрализуется аммиаком. Образующийся нитрат аммония NH4NO3 играет роль электролита-коагулятора. [39]
Получающийся при этом осадок пристает к стенкам стакана, плохо отфильтровывается и отмывается. Чтобы предотвратить гидролиз соли железа, раствор перед нагреванием подкисляют азотной кислотой, которая в процессе осаждения Fe3 нейтрализуется аммиаком. Образующийся нитрат аммония играет роль электролита-коагулятора. Ион Fe3 осаждают из достаточно концентрированного раствора, при этом аморфный осадок гидроксида железа ( Ш) получается менее объемистым, адсорбирует меньше примесей и легче отмывается от них. Чтобы еще более понизить адсорбцию осадком ионов С1 -, раствор после осаждения разбавляют 1 5 - 2-кратным объемом горячей воды. Промывая осадок, удаляют примеси С1, которые при прокаливании могут образовать с осадком летучий хлорид железа. [40]
Осадок практически не растворим в кислотах, но разлагается щелочами. Для подавления гидролиза солей железа реакцию ведут в кислой среде. [41]
Осадок практически нерастворим в кислотах, но разлагается щелочами. Для подавления гидролиза солей железа реакцию ведут в кислой среде. [42]
В производстве полосовой и листовой стали ( особенно жести) к качеству воды предъявляются повышенные требования. Однако с температурой растет гидролиз солей железа с выпадением в осадок гидроокиси и увеличивается скорость коррозии. После травления металла необходима промывка в холодной воде при температуре не выше 30 - 40 С или в теплой при 50 - 60 С. [43]
Ход работы, ( Работу ведут под тягой. К раствору прибавляют 2 5 - 3 мл H2SC4 для подавления гидролиза солей железа. [44]
Работу ведут под тягой. К раствору прибавляют 2 5 - 3 мл H2SO4 для подавления гидролиза солей железа. [45]
Страницы: 1 2 3 4