Гидролиз - сульфид
Cтраница 2
В литопоне определяют содержание сульфида цинка, являющегося пигментной частью ( сульфат бария - наполнитель), и содержание ухудшающей светостойкость литопона окиси цинка, образующейся вследствие гидролиза сульфида бария и окисления сульфида цинка при прокаливании. [16]
Остатки растворов после осаждения ионов сероводородом или сернистым аммонием нельзя сливать в канализационные раковины; они должны сливаться в особые банки со щелочью, связывающей H2S и полностью подавляющей гидролиз сульфидов. [17]
Гидролиз сульфида натрия Na2S протекает в две ступени, так как слабая кислота H2S двухосновная. [18]
При определенных условиях - значительном избытке сульфита натрия и пониженной щелочности котловой воды - может происходить образование сульфидов. Продуктом гидролиза сульфидов является сероводород, легко обнаруживаемый по запаху в пробах котловой воды. [19]
При гидролизе сульфида бора ( Ш) водой образуются борная кислота и сероводород. [20]
Значение гидролиза в качественном анализе - Реакции гидролиза широко используются в практике качественного анализа и позволяют разобраться в целом ряде сложных процессов. Так, гидролиз сульфидов алюминия, хрома и титана практически идет до конца, поэтому при действии на их соли сульфидом аммония в присутствии аммиачной буферной смеси ( NH4OH и NH4C1) вместо сульфидов A12S3, Cr2S3 и TiS. [21]
Реакции гидролиза широко используются в практике качественного анализа и позволяют разобраться в целом ряде сложных процессов. Так, гидролиз сульфидов алюминия, хрома и титана практически идет до конца, поэтому при действии на их соли сульфидом аммония в присутствии аммиачной буферной смеси ( NH4OH и NH4C1) вместо сульфидов A12S3, Cr2S3 и TiS2 образуются их гидроксиды А1 ( ОН) 3, Сг ( ОН) 3 и Ti ( ОН) 4, выпадение которых в виде осадка нельзя понять без знания гидролиза. [22]
Сернистые соединения азота при гидролизе выделяют аммиак и образуют кислородные кислоты серы. Напротив, при гидролизе сульфидов фосфора наряду с кислородными кислотами фосфора образуется сероводород. [23]
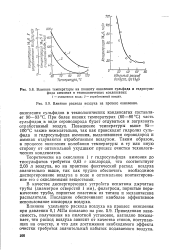 |
Влияние температуры на полноту окисления сульфида и гидросульфида аммония в технологических конденсатах.| Влияние расхода воздуха на процесс окисления. [24] |
Повышение температуры выше 95 - 100 С также нежелательно, так как происходит гидролиз сульфида и гидросульфида аммония, выделившиеся сероводород и аммиак отдуваются отработанным воздухом. Таким образом, в процессе окисления колебания температуры в ту или иную сторону от оптимальной ухудшают процесс очистки технологических конденсатов. [25]
Для щелочных и щелочноземельных металлов известны также гидросульфиды M HS и M2 ( HSh; гидросульфиды Са2 и Sr2 очень нестойки. Являясь солями слабой кислоты, растворимые сульфиды подвергаются гидролизу. Гидролиз сульфидов, содержащих металлы в высоких степенях окисления ( А125з, Cr2Ss и др.), часто идет до конца, он необратим. [26]
Существующий ГОСТ 1460 - 56 на карбид кальция не регламентирует количества серы в нем, а ограничивает содержание сероводорода в полученном из карбида ацетилене. Степень гидролиза сульфида кальция до сероводорода зависит от температуры и метода разложения карбида. [27]
Сульфатная варка дает определенные преимущества по сравнению с натронной. Сульфид натрия служит как бы резервной щелочью. По мере расходования NaOH на варку равновесие реакции гидролиза сульфида натрия сдвигается вправо. [28]
Сульфид ртути не растворяется в сильных и даже в концентрированных кислотах. Только царская водка легко растворяет его с образованием HgCl2 и серы. Сульфид ртути растворяется в растворах сульфидов щелочных металлов в присутствии гидроокисей этих металлов ( препятствуют гидролизу сульфида) с образованием тиосолей, например K2tHgS2 ] - 5H2O; он не растворяется в сульфиде аммония, так как концентрация сульфид-ионов слишком мала. Красный сульфид ртути менее растворим в сульфидах щелочных металлов, чем черный ( метастабильный); таким образом объясняют превращение черной формы моносульфида в киноварь под действием сульфидов щелочных металлов. [29]
Однако спрос на серную кислоту не только не снижается, а непрерывно растет, так как на смену старым потребителям приходят новые. Возрастает количество серной кислоты, используемой для производства фосфорной кислоты - сырья для получения концентрированных удобрений. Большие количества ее расходуются на производство оксида титана ( IV) [ титановую руду обрабатывают концентрированной серной кислотой и затем при гидролизе сульфида титана получают оксид титана ( IV) ], синтетических моющих веществ, некоторых химических волокон. [30]
Страницы: 1 2 3