Гидролиз - титан
Cтраница 1
Гидролиз титана в сернокислых титанилсульфатных растворах изучен достаточно подробно [ 1, с. [1]
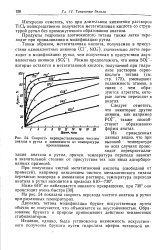 |
Скорость перекристаллизации чистого. [2] |
Продукты гидролиза азотнокислого титана также легко переходят при прокаливании в модификацию рутил. [3]
Фотометрический, гидролиз че-тыреххлористого титана в растворе серной кислоты и последующее определенно образовавшейся хлороводородной кислоты по реакции с нитратом серебра. [4]
Оценено влияние гидролиза титана на его экстракционное поведение. [5]
Изуче-ние условий гидролиза четыреххларистого титана с получением стандартной двуокиси титана, Отч. [6]
 |
Типы диаграмм плавкости титановых сплавов. [7] |
Вследствие образования комплексных соединений ТЮ2 х Н2О хорошо растворяется уксусной и винной кислотами; присутствие их в растворе препятствует гидролизу титана. [8]
Было найдено, что постоянство значений констант экстракции наблюдается в интервале кислотности до рН 0 7; отклонения при увеличении рН связаны, вероятно, с конкурирующим процессом гидролиза титана. [9]
Растворение сплава в разбавленных серной или соляной кислотах обеспечивает полное переведение титана в раствор, но при этом необходимо следить за тем, чтобы применяемые кислоты не содержали даже небольшой примеси азотной кислоты во избежание возможного гидролиза титана и, следовательно, его неминуемой потери для определения. [10]
Нейтрализованный раствор без замедления разбавляют примерно равным объемом горячей воды ( - 95) и в присутствии 1 мл 10 % - ного сульфосалицилата натрия титруют медленно, по каплям 0 05 М трилоном до полного исчезновения розового тона сульфосалицилата железа. Появляющаяся незначительная муть от гидролиза титана на результаты титрования не влияет. [11]
При отсутствии соединений свинца и сульфата бария и наличии двуокиси титана и силиката получаемый плав растворяют в растворе серной кислоты ( 1: 1) и нагревают до выделения густых белых паров серного ангидрида. Кремневая кислота выделяется в виде белого осадка, который отфильтровывают, предварительно разбавив водой. Во избежание гидролиза титана в растворе должно содержаться не менее 10 % серной кислоты. [12]
Так как экстракция проводится в щелочной среде, то присутствующий в растворе титан подвергается гидролизу, что мешает экстрагированию. Для устранения этого были проведены опыты по его маскированию с комплексонообразовате-лями: винной кислотой и глюкозой. Опыты показали, что винная кислота, хотя и устраняет гидролиз титана в щелочной среде, однако препятствует экстракции кальция, в то время как глюкоза, устраняя гидролиз, не создает помехи в экстракции. [13]
В водной среде титан образует соединения с карбоновьши и дикарбоновыми кислотами, оксикислотами и реагентами, имеющими несколько функциональных групп. Для всех соединений характерны связи Ti - О ( N, S, Р и др.), причем наиболее прочны соединения, имеющие структуру внутрикомплексных. Благодаря образованию комплексных соединений, гидроокись титана хорошо растворяется в уксусной и винной кислотах; присутствие этих кислот в растворе препятствует гидролизу титана. Но наиболее прочные комплексные соединения с титаном образует щавелевая кислота, которая, как и ее кислые соли - лучший растворитель свежеосаж-денной гидроокиси титана. При избытке щавелевой кислоты образуется титано-щавелевая кислота Н2 [ ТЮ ( С2О4) 2Ь2Н2О, устойчивая против гидролиза. Соль титано-щавелевой кислоты K2tTiO ( C2O4) 2 ], получить которую можно, растворяя гидроокись титана в растворе КНС2О4, перекристаллизовывается без гидролиза. [14]
В водной среде титан образует соединения с карбоновыми и дикарбоновыми кислотами, оксикислотами и реагентами, имеющими несколько функциональных групп. Для всех соединений характерны связи Ti - О ( N, S, Р и др.), причем наиболее прочны соединения, имеющие структуру внутрикомплексных. Благодаря образованию комплексных соединений, гидроокись титана хорошо растворяется в уксусной и винной кислотах; присутствие этих кислот в растворе препятствует гидролизу титана. Но наиболее прочные комплексные соединения с титаном образует щавелевая кислота, которая, как и ее кислые соли - лучший растворитель свежеосажденной гидроокиси титана. При избытке щавелевой кислоты образуется титано-щавелевая кислота Н2 [ ТЮ ( С2О4) 2 ] - 2Н2О, устойчивая против гидролиза. Соль титано-щавелевой кислоты К2 [ ТЮ ( С2О4) 2 ], получить которую можно, растворяя гидроокись титана в растворе КНС2О4, перекристаллизовывается без гидролиза. [15]
Страницы: 1 2